REDUÇÃO DE ATP INDUZIDA POR RADIAÇÃO E POSSÍVEL ENVOLVIMENTO DE SINALIZAÇÃO
Uma produção normal de ATP é mantida pela glicólise e pelo ciclo do TCA que ocorre nas mitocôndrias [99]. O ATP é a principal forma de energia para uma variedade de processos celulares, incluindo síntese de DNA, RNA e proteínas, manutenção do citoesqueleto, sinalização, transporte iônico e reparo. Aqui, relatamos que a lesão combinada reduziu significativamente o conteúdo de ATP celular no íleo, juntamente com o pâncreas, cérebro, baço, rim e pulmão [28]. A radiação exerce suas ações (1) diminuindo a piruvato desidrogenase (PDH, um complexo enzimático crucial para a conversão do piruvato em acetil CoA para entrada no ciclo do TCA), (2) aumentando a piruvato desidrogenase quinase (PDK, uma enzima que fosforila o PDH resultando em PDH tornando-se inativo) de modo que as mitocôndrias carecem de acetil CoA como combustível para gerar ATP [28] e (3) remodelação das mitocôndrias com fusão e fissão levando à proptose e autofagia [100]. Foi demonstrado que a MAPK desintegra a biogênese celular (101). Sabe-se que a redução induzida pela radiação nos níveis de ATP desintegra a estrutura e a função celular, levando à necrose, apoptose e autofagia (102–107).
É relatado que as poli (ADP-ribose) polimerases (abreviadas como PARP) reparam o DNA danificado e ativam a atividade do NF-κB que leva à inflamação e redução nos níveis de ATP. Sabe-se que o receptor ativado por proliferador de peroxissoma (PPPAR) -γ coativador-1α (PGC-1α) é regulado pela MAPK (108) e inibe a atividade do NF-κB (109). O aumento de PGC-1α induz a transcrição do fator respiratório nuclear (NRF) 1 e NRF2, levando à superexpressão de β-ATP sintase, citocromo c e citocromo c oxidase IV (110, 111). Além disso, o microRNA-696 inibe o PGC-1α (112). Como resultado, a produção de ATP aumenta e, assim, a apoptose e a necrose são inibidas (55, 113). Em nosso laboratório, descobrimos que a radiação isolada ou a lesão combinada com radiação diminui significativamente os níveis de ATP celular através da redução de NRF1 e NRF2 sem alteração de PARP e PGC-1α [Kiang et al., não publicado]. A Figura 2 mostra que a radiação isolada ou a lesão combinada ativa a atividade da MAPK, mas não estimula o PGC-1α. A radiação e a lesão combinada aumentam iNOS, RNS, NF-κB e citocinas, levando assim à diminuição da sobrevida. Ao mesmo tempo, a radiação e a lesão combinada reduzem NRF1, NRF2, β-ATP sintase, citocromo c e citocromo c oxidase IV. Como resultado, a produção de ATP é reduzida e subsequentemente ocorre a morte celular.
CONTRAMEDIDAS PARA LESÕES POR RADIAÇÃO E LESÕES COMBINADAS POR RADIAÇÃO
A FDA aprovou três medicamentos, nomeadamente, Neupogen, Neulasta e Leukine para a síndrome hematopoiética aguda [114]. Farese et al. [115] relataram que Neupogen diminuiu a mortalidade e a duração da neutropenia e trombocitopenia após irradiação corporal total de 7,5 Gy em primatas não humanos. Da mesma forma, Hankey et al. [116] relataram resultados semelhantes com o tratamento com Neulasta em primatas não humanos. Kiang et al. [29, 117] relataram que Neupogen e Neulasta diminuíram a mortalidade em camundongos após irradiação isolada de 9,5 Gy ou lesão combinada com radiação.
Um efeito sinérgico entre radiação e lesão traumática foi relatado em camundongos [15, 30, 37], ratos [38–42], porquinhos-da-índia [43], cães [44, 45] e suínos [118]. As principais características das lesões combinadas por radiação incluem: (a) choque, que ocorre mais cedo e é mais frequente e grave em comparação com lesões simples por radiação, muitas vezes tornando-se a principal causa de morte logo após a lesão; (b) supressão dramática da hematopoiese e do sistema imunológico, o que afeta negativamente o prognóstico após lesão combinada por radiação; (c) danos gastrointestinais extensos e graves, como ruptura da barreira mecânica e imunológica, que leva à disfunção na absorção e secreção e ao aumento do risco de infecção; e (d) atraso na cicatrização de feridas – muitas vezes o dobro do tempo de cicatrização apenas da ferida.
Uma vez que os mecanismos das lesões combinadas por radiação parecem ser mais complicados do que os mecanismos das lesões individuais isoladamente, pode-se esperar que os tratamentos também não sejam tão simples. DiCarlo et al. [119] sugere que a complexidade da resposta os torna pessimistas quanto à possibilidade de encontrar quaisquer tratamentos eficazes passíveis de utilização num cenário de vítimas em massa. No entanto, a busca por contramedidas farmacológicas para lesões combinadas por radiação tem se mostrado promissora.
Zou et al. [49] relatam que o bloqueio do nervo simpático cervical uma vez ao dia durante 14 dias após a lesão combinada por radiação diminui significativamente a mortalidade [120]. Ledney e Elliott [30] relataram que o imunomodulador inespecífico S-TDCM administrado i.p. imediatamente após a lesão combinada por radiação, juntamente com a aplicação sistêmica e tópica de gentamicina, melhora a sobrevida. Eles também relataram que o transplante de medula óssea singênico aumenta a sobrevivência de camundongos com lesões combinadas. Shah et al. [41] relataram que a grelina humana atenuou a lesão de órgãos e melhorou a sobrevivência em um modelo de radiação combinada com sepse em ratos. Nosso laboratório relatou que a grelina [10, 121, 122], Alxn4100TPO [123], ciprofloxacina [72, 124, 125] e células-tronco mesenquimais [10, 12] são eficazes para mitigar lesões combinadas por radiação. Na verdade, devido ao dano politraumático induzido pela radiação em múltiplos órgãos, abordagens de polifarmácia foram investigadas [29]. As possíveis interações entre medicamentos/produtos biológicos tratados precisam ser minuciosamente exploradas.
A resposta médica à exposição à radiação num cenário de vítimas em massa seria sempre diferente da forma como um pequeno número de vítimas expostas ou socorristas numa área contaminada com radiação são geridos em comparação com uma situação controlada envolvendo pacientes de radioterapia. É claramente irrealista, em situações de vítimas em massa, realizar bloqueios dos gânglios simpáticos cervicais, transplantes de medula óssea ou mesmo administrações intravenosas de medicamentos. Injeções intramusculares, medicamentos administrados por via oral e talvez injeções subcutâneas [126] podem ser os tratamentos mais complexos disponíveis para vítimas de vítimas em massa. As contramedidas para ataques de radiação ou acidentes nucleares que devem ser tomadas antes da exposição à radiação podem ser impraticáveis, uma vez que é bastante improvável que tal evento ocorra com aviso adequado; no entanto, as contramedidas podem revelar-se úteis em situações em que as exposições à radiação são bastante certas ou prováveis de acontecer conforme planeado, como no caso da radioterapia. O desenvolvimento bem-sucedido e a estratégia de contramedidas devem, portanto, abordar os requisitos específicos para um cenário de exposição à radiação de todos os tipos de situações possíveis de exposição à radiação.
POTENCIAIS BIOMARCADORES PARA RADIAÇÃO E LESÃO COMBINADA
Com uma vítima em massa após acidentes radiológicos ou detonação de armas nucleares, a triagem torna-se inevitável e desta necessidade surge a necessidade de biomarcadores facilmente acessíveis. Foi demonstrado que a IL-18 aumenta nas amostras de sangue de primatas não humanos [127], miniporcos [127] e camundongos [27, 127, 128]. Um perfil semelhante de IL-18 foi encontrado nas amostras de urina de primatas não humanos (129). Além disso, o G-CSF foi relatado como outro biomarcador confiável cujos níveis são aumentados pela radiação e lesão combinada por radiação [128, 130]. Isto é acompanhado por contagens reduzidas de linfócitos e aumento de ligantes de tirosina quinase (Flt-3) semelhantes a FMS em amostras de sangue de camundongos (130). A citrulina produzida pelos enterócitos é outro biomarcador que foi observado ser reduzido após lesão apenas por radiação e lesão combinada por radiação. A citrulina circulante pode servir como um biomarcador para lesão gastrointestinal aguda e prolongada em um primata não humano após irradiação corporal total e parcial (131).
MicroRNAs (miRs) foram investigados e sugeridos para regular proteínas e expressão gênica. Nas células humanas, a radiação pode regular positivamente o miR-30b, miR-30c e miR-30d, conforme observado nas células CD34 +, enquanto foi demonstrado que inibe a expressão do miR-30c nas células hFOB (132). Em primatas não humanos, a radiação pode aumentar o miR-574-5p, miR-126, miR-144, miR-21, miR-1-3p e miR-206 e diminuir os níveis de miR-150-5p (133). Em camundongos, a lesão combinada por radiação pode aumentar 8 miRNAs e diminuir 10 níveis de miRNAs no soro. Entre todos os miRNAs alterados, a lesão combinada por radiação aumentou particularmente os níveis de miR-34 no soro, resultando em aumento da fosforilação de ERK, p38 e aumento da sinalização de NF-κB, que regulam positivamente a expressão de iNOS e ativação de caspase-3 no íleo. Além disso, o let-7g/miR-98 tem como alvo o aumento da fosforilação de STAT3 no íleo, que é conhecido por se ligar à região promotora do gene iNOS. Além disso, sabe-se que MiR-15, miR-99 e miR-100 regulam IL-6 e TNF adequadamente [27]. Alterações em Let-7e, miR-30e e miR-29b foram relatadas associadas à regulação da hematopoiese e da inflamação [33]. O aumento nos níveis de miR-34a foi observado em camundongos expostos tanto ao campo misto (nêutrons e gama) quanto à radiação gama Co-60 [Kiang et al., não publicado]. Seria de grande interesse explorar se o miR-34a é regulado positivamente após irradiação com lesão combinada.
CONCLUSÃO
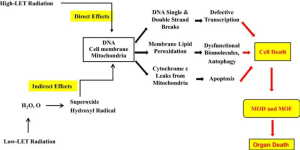
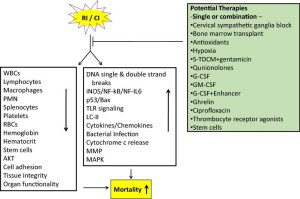
A radiação combinada com o trauma da ferida resulta numa diminuição dos níveis de linfócitos, macrófagos, neutrófilos, plaquetas, moléculas de adesão celular, integridade tecidual e células-tronco, mas leva a um aumento na atividade do iNOS/NF-kB/NF- Vias IL6 e p53/Bax, sinalização TLR, concentrações de citocinas (134), infecção bacteriana, liberação de citocromo c das mitocôndrias para o citoplasma e quebras de fita simples e dupla de DNA. Essas alterações levam à apoptose e autofagia, resultando em doenças/mortalidade. Lesão por radiação combinada com queimaduras, infecção ou fraturas pode ser mediada por mecanismos como aqueles observados após lesão por radiação combinada com traumatismo de ferida (Fig. 3). As contramedidas disponíveis para lesões combinadas por radiação são atualmente muito limitadas (Fig. 4), pelo que o desenvolvimento de agentes para prevenção, mitigação e tratamento continua a ser uma necessidade premente.
Figura 3
Representação simples da disfunção e falência de múltiplos órgãos e mortalidade resultante. LET transferência linear de energia, disfunção de múltiplos órgãos MOD, falência de múltiplos órgãos MOF.
A radiação e as lesões combinadas atenuam as defesas normais. Várias intervenções para tratar a radiação e lesões combinadas podem ser usadas isoladamente ou em combinação para melhorar a chance de sobrevivência em pacientes gravemente feridos.