EVIDÊNCIAS DO MUNDO REAL DE MAIS DE UM MILHÃO DE VACINAÇÕES COVID-19 SÃO CONSISTENTES COM A REATIVAÇÃO DO VÍRUS VARICELA-ZOSTER
INTRODUÇÃO
A doença de coronavírus 2019 (COVID-19), causada pela infecção pelo coronavírus 2 da síndrome respiratória aguda grave (SARS-CoV-2), tornou-se rapidamente uma pandemia, a partir da identificação dos primeiros casos. Globalmente, uma imensa esperança repousa na vacinação contra a COVID-19. A maioria das vacinas disponíveis atua apresentando a proteína spike viral (S) ao sistema imunológico do hospedeiro, produzindo uma imunização ativa pela indução de uma resposta humoral específica, seguida pela formação de anticorpos antivirais neutralizantes. Os soros contêm (i) mRNA que codifica a proteína S incorporada em nanopartículas lipídicas (LNPs), por exemplo, BNT162b2 da BioNTech/Pfizer ou mRNA-1273 da Moderna; (ii) vetores de adenovírus, como ChAdOx1 nCoV-19 da Astra-Zeneca, Ad26.COV2 da Johnson & Johnson. S ou Gam-COVID-19-Vac (Gamaleya National Center of Epidemiology and Microbiology); ou (iii) virions SARS-CoV-2 inativados, como na CoronaVac da Sinovac. Um amplo espectro de estudos clínicos realizados em diferentes países demonstrou altos níveis de proteção contra o COVID-19, especialmente no que diz respeito aos cursos graves da doença. Os perfis de segurança foram considerados aceitáveis, apesar da ocorrência de efeitos adversos menores, como dores musculares (mialgia), fadiga e outros sintomas semelhantes aos da gripe. No entanto, surgiram recentemente relatos de reações adversas medicamentosas (RAM) muito raras, porém graves, e eventos adversos medicamentosos (ADE). Especificamente, a doença pulmonar eosinofílica, trombose do seio venoso cerebral (CVST), embolia pulmonar, trombocitopenia imune induzida por vacina (VITT) e miocardite foram associadas à vacinação contra COVID-19.
Devido à rapidez com que a primeira geração de vacinas COVID-19 teve que ser desenvolvida, testada, produzida, entregue e finalmente utilizada, há uma necessidade urgente de rastrear coortes vacinadas para reações adversas ainda desconhecidas e efeitos indesejáveis; esses dados também são indispensáveis para refinar continuamente as vacinas de próxima geração. Embora qualquer relatório científico de riscos ou complicações possa ser mal interpretado (incluindo o presente trabalho), por exemplo, como parte de agendas anti-vacinas, acreditamos que é de fundamental relevância ética que potenciais RAMs/ADEs sejam meticulosamente investigados e divulgados ao público. Observe que muitos eventos adversos são conhecidos por ocorrer tanto com infecções (por exemplo, a própria COVID-19) quanto, em alguns casos, até mesmo com outras vacinas (não COVID): isto é, esses eventos adversos não são necessariamente efeitos colaterais específicos das várias vacinas COVID. Qualquer processo de tomada de decisão – seja uma recomendação de política para toda a população ou uma escolha individual/pessoal – é mais saudável se for equilibrado e informado por dados, ponderando as possíveis complicações relatadas aqui em relação aos benefícios significativos e bem estabelecidos da vacinação COVID-19.
Herpes zoster (HZ, sinônimo: herpes zoster) é uma doença infecciosa mucocutânea causada pela reativação do vírus varicela-zoster (VZV). A infecção inicial, muitas vezes contraída na infância, surge como uma erupção maculopapular (varíola, sinônimo: varicela). Apesar da recuperação clínica, o VZV persiste nos corpos das células neurais localizadas nos gânglios espinhais da raiz dorsal e nos gânglios do trigêmeo. Normalmente, o herpes se apresenta como uma erupção cutânea ou mucosa unilateral dolorosa que consiste em erosões confluentes após a formação de vesículas. O exantema/enantema normalmente corresponde a um dermátomo ou à área de inervação de um nervo sensitivo. O HZ é primariamente diagnosticado clinicamente e pode ser confirmado por reação em cadeia da polimerase (PCR) e ensaios imunossorventes ligados a enzimas (ELISA). O herpes zoster pode ser tratado com uma família de compostos análogos de nucleosídeos (aciclovir, valaciclovir e famciclovir) que inibem a DNA polimerase viral. Esses agentes virostáticos requerem administração imediata, idealmente dentro de 72 horas após o início da erupção cutânea. Além disso, uma vacina VZV está disponível.
Foi relatado que a reativação de herpesviridae, incluindo VZV, é potencialmente desencadeada por vacinas contra inter alia, febre amarela, hepatite A, raiva e influenza. Uma associação de HZ com a vacinação contra COVID-19 foi relatada em todo o mundo em relatos de casos e séries de casos, bem como em um estudo retrospectivo com foco na segurança do BNT162b2. Este último encontrou uma razão de risco (RR) de 1,43 com base em 15,8 eventos de HZ por 100.000 pacientes. Iwanaga et al. publicaram uma revisão narrativa de 399 pacientes que desenvolveram herpes zoster após a vacinação contra COVID-19, incluindo dois casos de HZ oral. Dentre eles, 24 indivíduos relataram histórico de varicela/HZ. Vinte indivíduos foram vacinados contra VZV. BNT162b2 foi mais frequentemente associado a HZ. Fathy et al. revisaram 35 casos de HZ após a vacinação contra COVID-19 relatados no Registro Internacional de Dermatologia. As bolhas ocorreram em proporções semelhantes após o uso de BNT162b2 e mRNA-1273.
Embora a HZ possa ser suficientemente tratada pela administração imediata de análogos de nucleosídeos, podem ocorrer complicações graves. Destes, os mais frequentes são infecções secundárias, o desenvolvimento de neuralgia herpética subaguda e neuralgia pós-herpética, bem como zoster oftálmico incluindo necrose retiniana aguda, que pode causar perda de visão. Complicações neurológicas potenciais bastante raras são síndrome de Hunt, síndrome de Guillain-Barré, paralisia de Bell, meningite asséptica, neuropatia motora periférica e mielite. Além disso, sabe-se que a VZV aumenta a morbidade materna em gestantes.
O presente trabalho busca determinar se uma associação entre a vacinação contra COVID-19 e a erupção do herpes zoster pode ser encontrada em uma grande coorte internacional, com base na análise estatística de dados do mundo real. Como hipótese de trabalho, assumimos que a incidência de HZ seria significativamente (detectável) maior em indivíduos vacinados contra COVID-19, versus aqueles que permaneceram não vacinados. Para coletar dados do assunto, foi usada a Rede de Pesquisa em Saúde Global TriNetX. Este banco de dados oferece grandes volumes de dados do mundo real agregados de vários centros; em novembro de 2021, o TriNetX incluiu registros médicos de mais de 250 milhões de indivíduos. Os dados clínicos da rede de pesquisa biomédica TriNetX são extraídos de mais de 120 organizações de saúde (HCO) em 19 países; reúne HCOs, contratar sites de pesquisa e empresas biofarmacêuticas para trocar dados clínicos longitudinais e fornecer análises de ponta. O recurso TriNetX foi usado recentemente para estudos retrospectivos de evidências do mundo real (RWE) de outros tópicos relacionados ao COVID-19. Aqui, descrevemos nossos achados para a reativação de VZV associada ao herpes, com base em uma pesquisa estatística de mais de 1 milhão de vacinas contra COVID-19.
MATERIAIS E MÉTODOS
Critérios de inclusão e exclusão
O banco de dados TriNetX foi acessado em 25 de novembro de 2021 e o período de elegibilidade foi limitado a 2 anos a partir da data de acesso. Assim, todos os pacientes que compareceram ao respectivo HCO para avaliação e atendimento neste período foram elegíveis para inclusão. Posteriormente, para construir as coortes iniciais, o banco de dados foi pesquisado para (i) indivíduos que receberam pelo menos uma injeção intramuscular de mRNA LNP ou vacina COVID-19 baseada em vetor de adenovírus (dando Coorte I) e (II) aqueles que foram não vacinados contra COVID-19 (dando Coorte II).
Processo de correspondência
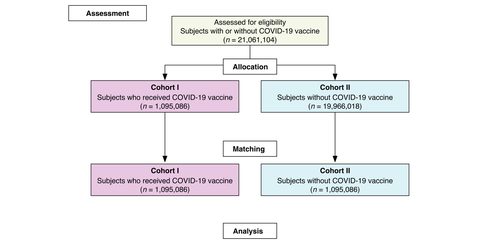
A fim de mitigar o viés de confusão por meio do método de correspondência de pontuação de propensão, subcoortes estratificadas e balanceadas nas distribuições de idade e gênero atuais foram construídas a partir das coortes iniciais, conforme mostrado na Fig. 1. A correspondência um-para-um foi realizada para replicar as condições aleatórias o mais próximo possível.
Análise estatística
Definimos o desfecho primário como “herpes zoster” diagnosticada clinicamente (Código B.02 da Classificação Internacional de Doenças (CID) 10), sendo essa condição atendida (i) dentro de 1 a 60 dias após a vacinação com COVID-19 (para a Coorte I) ou (II) dentro de 1 a 60 dias após a visita de um paciente ao HCO por qualquer outro motivo (para a Coorte II). Em seguida, essa estrutura foi usada para conduzir uma análise de Kaplan-Meier e as razões de risco (RRs) e as razões de chances (ORs) foram calculadas. Além disso, ambas as coortes foram testadas para diferenças de distribuição em relação à história de radioterapia e/ou quimioterapia, imunossupressão iatrogênica, bem como infecção assintomática e sintomática com o vírus da imunodeficiência humana (HIV; códigos CID-10 Z21 e B20). As análises estatísticas foram realizadas usando o teste de log-rank, em que o limite de significância foi definido como P ≤ 0,05.
Aprovação ética
Todos os métodos foram executados em conformidade com as diretrizes e regulamentos relevantes. Todos os HCOs dos quais os dados foram transferidos para o TriNetX obtiveram o consentimento informado (por escrito) de todos os pacientes e/ou seus responsáveis legais. O TriNetX está em conformidade com o Health Insurance Portability and Accountability Act (HIPAA), que é a lei federal dos EUA que protege a privacidade e a segurança dos dados de saúde. A TriNetX é certificada pela norma ISO 27001:2013 e mantém um Sistema de Gerenciamento de Segurança da Informação (ISMS) para garantir a proteção dos dados de saúde aos quais tem acesso e para atender aos requisitos da Regra de Segurança HIPAA. Quaisquer dados exibidos na plataforma TriNetX de forma agregada ou quaisquer dados em nível de paciente fornecidos em um conjunto de dados gerado pela plataforma TriNetX contêm apenas dados não identificados, de acordo com o padrão de desidentificação definido na Seção §164.514(a) da Regra de Privacidade da HIPAA. O processo pelo qual os dados são desidentificados é atestado por meio de uma determinação formal por um especialista qualificado, conforme definido na Seção §164.514(b) (1) da Regra de Privacidade da HIPAA. Esta determinação formal por um especialista qualificado, atualizada em dezembro de 2020, substitui a necessidade de renúncia anterior da TriNetX do Western Institutional Review Board (IRB). A rede TriNetX contém dados fornecidos por organizações de assistência médica (HCOs) participantes, cada uma das quais representa e garante que tem todos os direitos, consentimentos, aprovações e autoridade necessários para fornecer os dados à TriNetX sob um acordo de associação comercial (BAA), desde que seu nome permaneça anônimo como fonte de dados e seus dados sejam utilizados para fins de pesquisa.
RESULTADOS
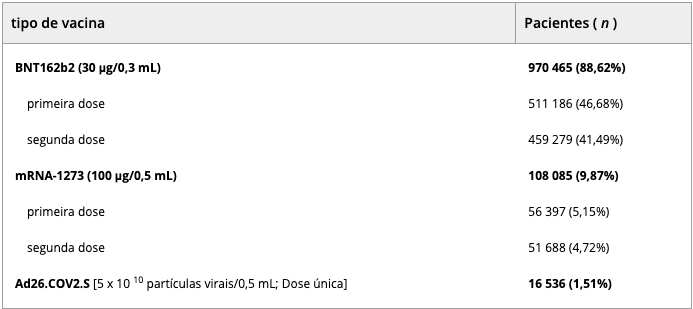
Com base nos critérios de inclusão e exclusão, 1.095.086 e 16.966.018 pacientes foram elegíveis para compor as Coortes I e II, respectivamente. Após o processo de pareamento, cada Coorte contabilizou 1.095.086 indivíduos. As características demográficas dos sujeitos incluídos são apresentadas na Tabela 1 e as frequências das vacinas aplicadas na Coorte I são apresentadas na Tabela 2.
Tabela 1. Características dos pacientes antes e depois da correspondência das coortes I (código CID-10 B.02 após vacinação contra COVID-19) e II (código CID-10 B.02 sem vacinação contra COVID-19)
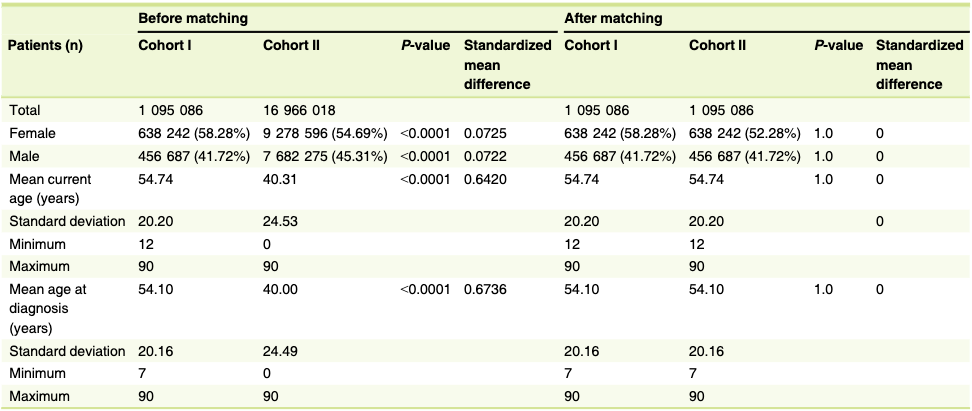
Tabela 2. Tipos de vacinas COVID-19 aplicadas na Coorte I
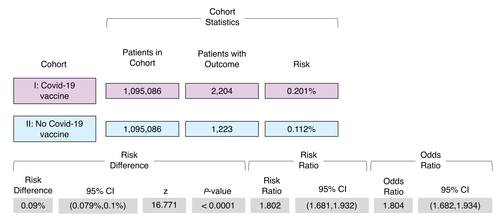
Entre os indivíduos da Coorte I, 2.204 indivíduos desenvolveram HZ dentro de 60 dias após a vacinação contra COVID-19 (Fig. 2). Enquanto isso, na Coorte II, encontramos 1.223 pacientes diagnosticados com HZ dentro de 60 dias após terem visitado um HCO por qualquer outro motivo. O risco de desenvolver herpes zoster foi calculado como 0,20% vs. 0,11% para as Coortes I e II, respectivamente. A diferença de risco subjacente de 0,09% foi estatisticamente altamente significativa (P <0,0001; intervalo de confiança de 95% (IC) = 0,079%; 0,100%). Os valores calculados de RR e OR (Fig. 2) foram 1,802 (95% CI = 1,680; 1,932) e 1,804 (95% CI = 1,682; 1,934), respectivamente.
Os dados do paciente sobre um histórico de radioterapia e quimioterapia, imunossupressão iatrogênica, bem como infecção assintomática e sintomática com HIV (CID-10 códigos Z21 e B20), estavam disponíveis para 641.277 indivíduos de ambas as coortes. As frequências de história de radioterapia ou quimioterapia foram significativamente maiores na Coorte II, sendo as diferenças (para a Coorte I vs. II): radioterapia = 10 vs. 41; quimioterapia = 1020 vs. 2219 indivíduos (P ≤ 0,05). Em relação ao uso de imunossupressores e prevalência dos códigos CID-10 relacionados ao HIV (Z21 e B20), não foram detectadas diferenças significativas (P > 0,05).
DISCUSSÃO
O presente estudo procurou determinar se a frequência de diagnósticos de herpes-zoster era maior entre os pacientes que receberam vacinas contra COVID-19 (Coorte I) versus aqueles que não foram vacinados (Coorte II). Antecipamos que a incidência de HZ pode ser detectavelmente maior na Coorte I vs. Coorte II, com base em relatórios anteriores de outros e no que é geralmente conhecido sobre fenômenos de reativação de herpes viridae. A hipótese foi confirmada, com base na análise comparativa de um período de 60 dias após a vacinação (para Coorte I) vs. o mesmo período de tempo após uma visita ao HCO por qualquer outro motivo (Coorte II). Consequentemente, a reativação do vírus herpes-zoster parece ser uma RAM potencial para vacinas COVID-19, pelo menos para formulações baseadas em mRNA LNP. Esse achado concorda com relatórios recentes (citados na Introdução), uma diferença significativa sendo que o presente trabalho está em uma escala mais ampla (volume de casos e distribuído internacionalmente) versus o que foi amostrado em outros relatórios recentes. No entanto, não podemos tirar conclusões de nossa análise das vacinas baseadas em vetores (vs baseadas em mRNA), pois apenas 1,51% dos indivíduos da Coorte I receberam Ad26.COV2.S.
Curiosamente, uma incidência geralmente aumentada de infecções pelo vírus da herpes foi relatada desde o início da pandemia de COVID-19. Foi levantada a possibilidade de que a reativação do herpes viridae possa ser desencadeada por efeitos supressores do SARS-CoV-2 no sistema imunológico do hospedeiro; além disso, observou-se que o estresse psicológico relacionado à pandemia também desempenha um papel causal. Por outro lado, a vacinação contra a COVID-19 parece potencialmente aumentar o risco de precipitar HZ. Embora os mecanismos moleculares específicos que causam a reativação do VZV permaneçam desconhecidos, alguns fatores de risco foram identificados – incluindo estresse, idade elevada, uso de imunossupressores, quimioterapia e radioterapia. Um fio condutor entre essas condições é que elas correspondem a uma diminuição da competência imunológica, em termos de imunoglobulinas, linfócitos T CD4+ e CD8+ e células T de memória. No contexto do presente estudo, observamos que falhas imunes inatas ou mediadas por células, causadas pela resposta de um hospedeiro à vacinação contra COVID-19, foram levantadas como fatores potencialmente causadores da reativação do VZV. Psicogiou et al. postulou uma incapacidade temporária das células T CD8+ específicas do VZV, permitindo que o VZV se reativasse e, assim, causasse HZ.
Tanto a probabilidade de cursos graves da doença quanto os riscos das complicações listadas aumentam com o aumento da idade devido à imunossenescência adaptativa; a respeito, a imunossenescência foi associada não apenas a uma suscetibilidade aumentada a infecções virais, mas também a uma resposta diminuída à vacinação. Isso levanta um problema que é uma fonte de informação potencialmente benéfica (paciente por paciente): aqueles que apresentam reativação do VZV após a imunização contra a COVID-19 podem ter uma taxa de proteção menor contra a COVID-19. Além disso, pode valer a pena considerar se a vacinação para VZV, ou mesmo o uso profilático de drogas análogas de nucleosídeos, pode ser aplicada em pacientes com alto risco de reativação de VZV, especialmente para pacientes acima de 60 anos. Considerando tudo o que foi dito acima, reiteramos que, no geral, os benefícios gerais da vacinação contra a COVID-19 superam em muito os riscos potenciais para uma vasta preponderância da população.
Além das restrições inerentes à sua natureza retrospectiva (por exemplo, indisponibilidade de um braço placebo/coortes de controle), o estudo aqui relatado não está isento de certas limitações; trabalho futuro pode procurar abordar essas questões. Por exemplo, dados sobre níveis de estresse psicoemocional, histórico de vacinação VZV e histórico de varíola podem ser altamente valiosos para incluir neste tipo de análise. Da mesma forma, dados sobre o uso de imunossupressores ou a presença de doenças gerais que causam imunodeficiência (especialmente infecção pelo HIV) e histórias de quimioterapia e/ou radioterapia foram fornecidos para um número limitado de pacientes, mas informações detalhadas de histórico não estavam disponíveis para inclusão na presente análise. Para superar essas limitações, estudos futuros podem considerar o uso de um desenho prospectivo padrão (controlado por placebo, randomizado, duplo-cego) para avaliar e ampliar os resultados aqui relatados.
RECONHECIMENTOS
Financiamento de Acesso Aberto habilitado e organizado pelo Projekt DEAL.