O Fenbendazol mata as células cancerígenas responsáveis por matar pacientes com câncer.
por Ben Fen
Um estudo recente de 2022 publicado na revista científica Breast Cancer Research descobriu que o mebendazol (fenbendazol), um medicamento seguro, prontamente disponível, barato e livre de efeitos colaterais que tem décadas de dados favoráveis de segurança e eficácia, previne e erradica o câncer de mama triplo negativo e também previne o desenvolvimento de metástases, reduzindo a probabilidade de desenvolvimento de células-tronco cancerígenas em regiões distantes.
Você sabia que nem todas as células cancerígenas são criadas iguais? Existe um processo pelo qual as células cancerosas mudam, seja devido a tratamentos destinados a ajudar, à genética e/ou à passagem do tempo (provavelmente uma interação de um ou mais fatores acima mencionados e outros fatores ainda a serem identificados), em que as células cancerígenas se tornam mais letais (Brash, 2019, por exemplo). De acordo com Greaves & Maley (2012) a quimioterapia contra o câncer mata algumas células tumorais, mas muitas vezes cria clones resistentes à quimioterapia. As células-tronco cancerosas são particularmente preocupantes porque essas células desempenham funções de iniciação e propagação do câncer que são características da disseminação metastática de um local para outro (Greaves & Maley, 2019). A maioria das mortes por câncer é causada por estas células geradas, terapeuticamente resistentes aos tratamentos convencionais, que depois colonizam e perturbam o funcionamento de órgãos distantes.
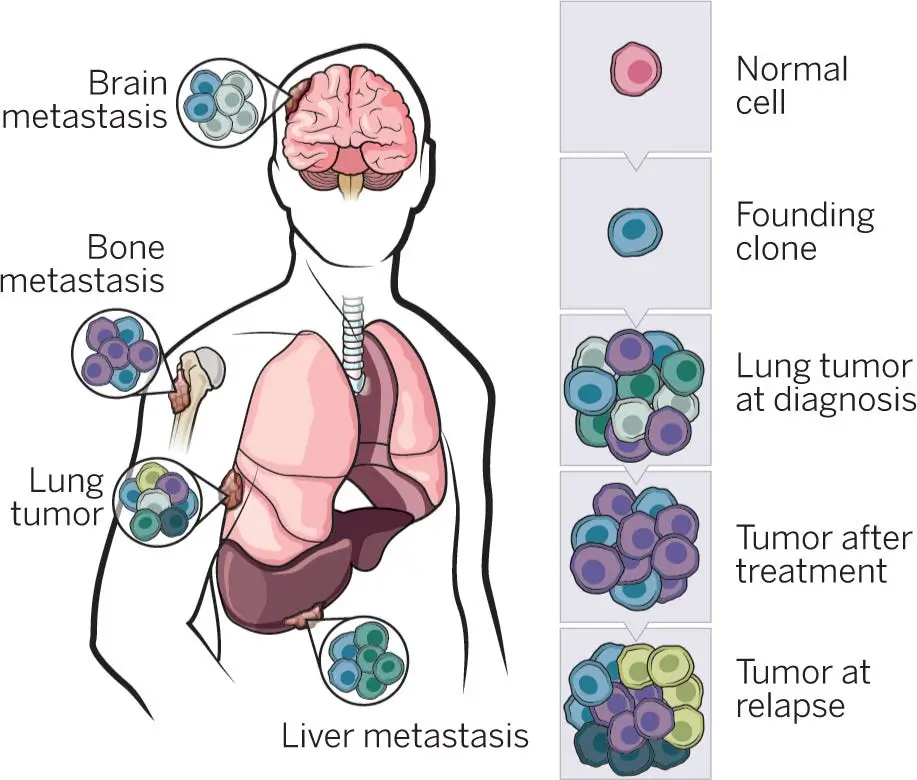
Ataque dos clones. A figura acima é uma representação gráfica de como as células tumorais podem mudar em função do tratamento e do tempo. O tumor original pode mudar de uma massa relativamente homogênea de clones para uma massa heterogênea mais complexa de células que contém clones, clones refratários e células-tronco cancerígenas. Geralmente são esses tumores mais complexos e heterogêneos os responsáveis pelas mortes por câncer. Extraído de Govidan (2014).
A maioria dos tratamentos contemporâneos contra o câncer, sejam eles químicos ou radiológicos, são eficazes no tratamento da maioria dos clones de células cancerígenas de primeira geração, também conhecidos como clones fundadores. Infelizmente, esses tratamentos são totalmente ineficazes no tratamento de células-tronco cancerígenas ou clones refratários que eles criam (Zhou, 2016), e “não há medicamentos aprovados para atingir especificamente esta população de células” de células-tronco cancerígenas (Guerini et al., 2019).
Até agora.
Uma elegante série de experimentos do laboratório de Riggin na Universidade Johns Hopkins demonstrou que doses fisiológicas de mebendazol (fenbendazol) erradicaram várias formas de câncer de mama, incluindo câncer de mama triplo negativo e, o mais importante para este artigo específico da Substack, o mebendazol também foi eficaz na redução ou eliminação de metástases em órgãos distantes (Joe et al., 2022).
O câncer de mama é o câncer mais comum entre as mulheres e, a cada ano, causa mais de 500.000 mortes em todo o mundo, com cerca de 2 milhões de novos casos diagnosticados a cada ano, de acordo com Cancer.org. Existem diferentes formas de câncer de mama caracterizadas por subtipos moleculares e histológicos. Para determinar que tipo de câncer de mama está presente, os patologistas usam técnicas de coloração imuno-histoquímica para determinar a presença ou ausência de dois receptores hormonais (HR), um é o receptor de progesterona (PR) e o outro é o receptor de estrogênio (ER), bem como o receptor 2 do fator de crescimento epidérmico humano (HER2) (Taherian-Fard et al., 2014, por exemplo). Embora existam quimioterapias tradicionais direcionadas para pacientes com doença HR+/HER2−, HR+/HER2+, HR−/HER2+, o câncer de mama triplo-negativo não possui receptores HR e HER2, tornando as terapias ER e HER2 ineficazes (Newton et al., 2022).
Por que o câncer de mama triplo negativo é especialmente letal
Como esse tipo de câncer de mama não possui os receptores hormonais usados pelos medicamentos atuais para atacar outros tipos de câncer de mama, o prognóstico é muito ruim. Além disso, o câncer de mama triplo negativo é agressivo e muitas vezes leva a metástases ósseas, cerebrais, hepáticas e pulmonares. Devido à tendência do câncer de mama triplo negativo de metastatizar, Joe et al., (2022) pensaram que seria um bom tipo de câncer para testar se o mebendazol seria seguro e eficaz na prevenção de metástases.
Usando uma variedade de modelos in vitro (placa de Petri) e in vivo (animais vivos), Joe et al., (2022) mostraram que o mebendazol preveniu o desenvolvimento de câncer de mama triplo negativo e erradicou o câncer de mama triplo negativo previamente estabelecido, reduziu a metástase pulmonar à distância, evitando metástase hepática. Além disso, o tratamento com mebendazol levou a uma redução dramática no marcador celular Integrina β4 (ITGβ4), que está ligado ao desenvolvimento de células-tronco cancerígenas em locais distantes.
O mebendazol previne e erradica as células do câncer de mama triplo negativo (TNBC) e também interrompe ou bloqueia a propagação dessas células.
Estas experiências examinaram os efeitos do mebendazol sobre fatores associados à migração de células cancerígenas e mediram alterações nos genes que estão associados à migração celular pelo mebendazol.
O mebendazol previne o crescimento do TNBC e mata o TNBC estabelecido – Primeiro, eles replicaram o efeito primário do mebendazol nas células de câncer de mama triplo negativas. De uma forma dependente da dose, o mebendazol preveniu o crescimento de células TNBC humanas e matou colônias estabelecidas de células TNBC humanas (ver Joe et al., 2022, Figura 1). O mebendazol, em doses fisiológicas humanas usadas para matar parasitas, também previne e mata as células TNBC. UMA GRANDE DESCOBERTA! Discutiremos mais sobre as implicações dessa descoberta posteriormente.
O mebendazol reduz a migração de células TNBC humanas numa placa de Petri (in vitro) – Em seguida, avaliaram os efeitos do mebendazol na capacidade migratória das células TNBC humanas. Uma experiência envolveu o crescimento de células TNBC num receptáculo de meio de crescimento até que toda a superfície estivesse revestida com células TNBC (cerca de 48 horas). Em seguida, eles rasparam um canal das células e registraram o que acontece sob várias doses fisiológicas de mebendazol versus placebo. A questão é: as células TNBC voltam a crescer e, se isso acontecer, com que rapidez? O mebendazol preveniu o novo crescimento das células TNBC de uma forma dependente da dose, medida 24 horas depois. Ainda analisando a migração celular, o experimento seguinte examinou os efeitos do mebendazol na capacidade das células TNBC de migrar de um lugar para outro. Novamente, numa placa de Petri (uma experiência fora do corpo), descobriram que o tratamento prévio com mebendazol reduziu a capacidade das células TBNC migrar de um local para outro na placa de Petri.
Este experimento justificou os experimentos de acompanhamento descritos a seguir para descobrir como o mebendazol interrompe a migração de células TNBC. E o mebendazol faz a mesma coisa em um modelo biológico vivo de TNBC?
O mebendazol interrompe o ciclo celular replicativo e mata o TNBC em 72 horas – Em seguida, eles examinaram como as células TNBC foram mortas pelo mebendazol. Ao medir várias enzimas associadas a várias fases da divisão celular, Joe et al. (2022) descobriram que o mebendazol aumentou muito a quinase 1 dependente de ciclina fosforilada (CDK1) e a ciclina-B1 (CCNB1), indicativa de parada do ciclo celular G2/M. Basicamente, o mebendazol impede que as células TBNC se dividam ou se repliquem. O que é realmente interessante é que o mebendazol causou a parada do ciclo celular, também conhecida como divisão celular, em 48 horas e as células TNBC morreram em 72 horas.
O mebendazol interrompe o crescimento do tumor TNBC e previne metástases em órgãos distantes em camundongos – Camundongos fêmeas foram injetados com células TNBC humanas em regiões mamárias. Os tumores foram deixados para crescer durante 5 dias. Em seguida, os ratos foram colocados aleatoriamente em grupos tratados com mebendazol ou em um grupo controle com placebo. IMPORTANTE: os ratos foram alimentados com mebendazol por via oral. Importante porque os humanos que se autotratam com fenbendazol o tomam por via oral. Os camundongos receberam mebendazol na ração (215 ppm de mebendazol na ração 7 dias por semana – grupo FEED), 20 mg/kg de mebendazol em óleo de gergelim administrado por via oral (por gavagem, que é alimentado por um tubo pela garganta até o estômago). 4x/semana para garantir que seja ingerido) e 30 mg/kg, 4x/semana por grupo de gavagem.
Quarenta e um dias depois, os ratos foram sacrificados e os tumores foram examinados. Ambos os grupos FEED e 30mg/kg de mebendazol tiveram tumores 35% e 55% menores que o grupo controle ao final dos 41 dias.
Então, medindo a quantidade de DNA humano em outros órgãos (lembre-se de que as células TNBC injetadas nos camundongos eram de origem humana), uma medida da carga metastática pode ser obtida. Os grupos FEED e 30 mg/kg de mebendazol tiveram uma carga metastática diminuída em 60% e 72%, respectivamente, conforme medido pela quantidade de DNA humano nos pulmões.
Para replicar mais de perto o que pode acontecer em ensaios clínicos em humanos, outro experimento foi conduzido implantando primeiro células TNBC nas regiões mamárias dos camundongos. Em seguida, os ratos foram colocados no protocolo FEED com mebendazol durante 5 semanas. Em seguida, os tumores foram removidos cirurgicamente (como poderiam ser em condições humanas comparáveis) e os camundongos viveram mais duas semanas após a cirurgia no protocolo FEED, após o qual os camundongos foram sacrificados e a propagação do TNBC foi medida pelo conteúdo de DNA humano em os pulmões e o fígado.
Os ratos alimentados com mebendazol apresentaram tumores mamários dramaticamente menores às 5 semanas e significativamente menos evidências metastáticas nos pulmões e nenhuma evidência de disseminação metastática para o fígado em comparação com os controles. Para que não haja mal-entendidos, citaremos os autores: “Os resultados demonstraram que o mebendazol reduz as metástases pulmonares em maior extensão do que inibe o crescimento do tumor e o mebendazol abole completamente as metástases hepáticas”. Joe e outros, (2022) p15.
O mebendazol reduz células-tronco cancerígenas – Em um esforço para compreender o mecanismo de como as metástases à distância foram reduzidas pelo mebendazol, Joe et al. (2022) examinaram como os genes conhecidos por estarem envolvidos na disseminação metastática do TNBC foram afetados pelo mebendazol. Eles descobriram que o gene que codifica a Integrina β4 (ITGβ4) é bastante reduzido pelo mebendazol. Foi demonstrado que a integrina β4 é um marcador ou fator intimamente associado às células-tronco cancerígenas (Bierie et al., 2017). Eles também descobriram que marcadores adicionais de células-tronco cancerígenas (células CD44hiCD24low) também foram reduzidos pelo mebendazol.
Resumo
Há muito para desvendar aqui, mas não vamos sair do caminho principal: parece certamente que existem provas contundentes de que o mebendazol (fenbendazol) erradica o câncer. Este também parece ser o primeiro artigo a descrever a capacidade do mebendazol de erradicar, mas também de PREVENIR o câncer de mama triplo negativo. Esta é a principal descoberta nº 1. Um artigo anterior de 2019 descreveu como o mebendazol melhorou (potenciava) os efeitos terapêuticos da radiação ionizante no TNBC (Zhang et al., 2019).
A primeira experiência descrita acima replicou a observação principal de que o mebendazol (fenbendazol) é eficaz na erradicação e prevenção do câncer da mama. E não qualquer câncer de mama, mas câncer de mama triplo negativo. O TNBC é considerado particularmente letal porque não possui os receptores hormonais através dos quais funcionam as quimioterapias tradicionais. Essencialmente, tornando as células TNBC invisíveis à quimioterapia tradicional. O artigo de Joe et al. (2022) afunda este navio conceitual no fundo do oceano. Como o câncer de mama é categorizado em subtipos como HR+/HER2−, HR+/HER2+, HR−/HER2+ com base nos tratamentos convencionais disponíveis para atacá-los, um sistema de classificação falso e enganoso foi desenvolvido e usado para orientar o tratamento. Porque se o mebendazol parece matar todos os tipos de câncer de mama comumente encontrados, incluindo o temido TNBC, a classificação dos cânceres de mama em subtipos com base na presença de receptores hormonais é uma distinção sem diferença funcional na presença de mebendazol. Esta é a principal descoberta nº 2.
O TNBC é considerado agressivo porque é provável que se espalhe e as células TNBC que se espalham têm qualidades distintas adicionais que as tornam impermeáveis aos tratamentos quimioterápicos tradicionais. Joe e outros. (2022) mostram que o mebendazol prejudica a disseminação à distância do TNBC e identificam um mecanismo de como isso acontece (regulando negativamente o gene associado ao crescimento de células-tronco cancerígenas). Além de matar o TNBC, o mebendazol provavelmente também matará as células TNBC que migraram! Esta é a principal descoberta nº 3. Além disso, considerando uma aplicação prática à luz de Joe et al., (2022), não deveriam todos os pacientes com câncer de mama recentemente diagnosticados, especialmente pacientes com TNBC, receber imediatamente doses terapêuticas de mebendazol para prevenir a propagação metastática? Pelo menos? O estudo de Joe et al. (2022) foi publicado na revista Breast Cancer Research! Todos os profissionais médicos do câncer de mama provavelmente estão cientes do artigo de Joe et al. (2022).
Joe et al., (2022) foram deliberados no uso de doses fisiológicas de mebendazol. Estas doses correspondem estreitamente às doses terapêuticas utilizadas como antiparasitário e às doses que as pessoas utilizam para autotratar os seus próprios cânceres com fenbendazol, 222 mg a 888 mg/dia.
Houve uma nota processual aparentemente menor em Joe et al. (2022) que foi oferecido para explicar por que a eficácia do mebendazol foi maior na erradicação do TNBC nas mãos em comparação com um estudo anterior (Zhang et al., 2019). Os autores apontaram que administraram mebendazol por via oral a camundongos em uma dieta rica em gordura ou por gavagem em uma suspensão de óleo de gergelim (Joe et al., 2022, pág. 17), o que pode ser responsável pela maior eficácia terapêutica observada (ver Liu et al., 2012).
Pensamentos finais
Neste mundo invertido e atrasado do mebendazol (fenbendazol) e da pesquisa sobre o câncer, aqueles que sofrem de câncer mal podem esperar que os médicos e a política alcancem o estado da arte, isto é, perceber e admitir que o Fenbendazol Cura o Câncer. Todos os relatos de casos neste substack e em outros lugares usam fenbendazol para erradicar seus cânceres. Como os estudos pré-clínicos de câncer como Joe et al., (2022) usam mebendazol (ironicamente a forma humana de fenbendazol) e os humanos autotratam seus cânceres com fenbendazol (a forma animal de mebendazol), é muito razoável supor que mebendazol e fenbendazol são equivalentes funcionais em relação ao câncer. Os dados humanos, recolhidos à medida que as pessoas autotratam os seus cânceres, exercendo o direito de experimentar medicamentos que salvam vidas, como o fenbendazol, demonstram que os efeitos do fenbendazol na erradicação de vários cânceres são previsíveis e nada surpreendentes, dada a riqueza de pesquisas básicas e pré-clínicas anteriores como essa de Joe et al., (2022).
O fenbendazol tem como alvo até os cânceres mais incuráveis, como o TNBC. O fenbendazol erradica as células-tronco cancerígenas que podem ser geradas por tratamentos quimioterápicos tradicionais. Em alguma ironia perturbadora e doentia, o fenbendazol é uma cura para os cânceres que os tratamentos tradicionais contra o câncer causam! Precisamos de determinar as condições sob as quais os efeitos terapêuticos do fenbendazol sobre o câncer podem ser otimizados. A dosagem, o método de administração, o tempo de aplicação e os agentes sinérgicos para otimizar a eficácia do fenbendazol podem ser determinados dentro de 6 meses, se assim desejarmos.
Temos a cura para o câncer. O que falta é a coragem e a vontade política para aplicar esse conhecimento de uma forma altruísta para ajudar aqueles que desesperadamente não podem esperar.
(É importante notar que vários dos protocolos experimentais utilizados aqui não foram otimizados para matar todas as células TNBC, apenas para prejudicar o seu crescimento ou propagação para efeitos da experiência específica).
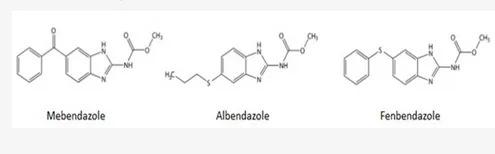
Fenbendazol vs. Mebendazol vs. Albendazol vs. Flubenzadol: Os benzimidazóis são quimicamente muito semelhantes e têm mecanismos de ação muito semelhantes no que diz respeito à interrupção da função dos microtúbulos, especificamente definida como a ligação ao local sensível à colchicina da subunidade beta da tubulina helminítica (parasita), interrompendo assim a ligação dessa unidade beta com o unidade alfa de tubulina que bloqueia o transporte intracelular e a absorção de glicose (Guerini et al., 2019). Se alguém lhe perguntar como o fenbendazol mata as células cancerígenas, a resposta está em itálico na frase anterior.
A classe de medicamentos conhecidos como benzimidazóis inclui fenbendazol, mebendazol, albendazol e flubendazol. O mebendazol é a forma aprovada para uso humano, enquanto o fenbendazol é aprovado para uso veterinário. A principal diferença é o custo. O mebendazol custa em torno de US$555 por comprimido de 100 mg, enquanto o fenbendazol é barato ~48 centavos por dose de pó livre de 222 mg (Williams, 2019). Como você deve se lembrar, o albendazol é a forma usada para tratar parasitas intestinais na Índia e custa 2 centavos por comprimido. Para sua informação, para ilustrar como os americanos são enganados pela Big Pharma, dois comprimidos de mebendazol custam apenas US$ 4 no Reino Unido, 27 centavos por comprimido de 100 mg na Índia e US$ 555 por comprimido de 100 mg nos EUA.
Embora a maior parte da pesquisa pré-clínica use mebendazol, provavelmente porque é a forma de fenbendazol aprovada pela FDA para humanos, praticamente todos os relatórios clínicos de autotratamento envolvem o uso de fenbendazol. Dado que os estudos pré-clínicos sobre o câncer utilizam mebendazol (ironicamente a forma humana do fenbendazol) e os seres humanos autotratam os seus cânceres com fenbendazol (a forma animal do mebendazol), é muito razoável assumir que o mebendazol e o fenbendazol são equivalentes funcionais no que diz respeito ao câncer. Seria útil se futuras investigações utilizassem simplesmente o fenbendazol como uma questão prática. Para os fins desta Substack, fenbendazol, mebendazol e albendazol são usados de forma intercambiável.
Referências
Bierie B, et al. (2017). Integrina-β4 identifica populações enriquecidas com células-tronco cancerígenas de células de carcinoma parcialmente mesenquimais. Proc Natl Acad Sci. doi: 10.1073/pnas.1618298114. (Artigo gratuito do PMC])
Brash DE (2019). Acelerando o câncer sem mutações. eLife, 8, e45809. https://doi.org/10.7554/eLife.45809
Govindan, R. (2014) Ataque dos clones. Ciência, 346, 169-170 (2014).DOI:10.1126/science.1259926
Greaves, M. e Maley, CC (2012). Evolução clonal no câncer. Natureza, 481(7381), 306–313. https://doi.org/10.1038/nature10762
Guerini, A. E., Triggiani, L., Maddalo, M., Bonù, M. L., Frassine, F., Baiguini, A., Alghisi, A., Tomasini, D., Borghetti, P., Pasinetti, N., Bresciani, R., Magrini, SM e Buglione, M. (2019). Mebendazol como candidato para reaproveitamento de medicamentos em oncologia: uma extensa revisão da literatura atual. Cânceres, 11(9), 1284. https://doi.org/10.3390/cancers11091284
Joe, NS, Godet, I., Milki, N., Ain, NU I., Oza, HH, Riggins, GJ, & Gilkes, DM (2022). O mebendazol previne metástases em órgãos distantes, em parte, diminuindo a expressão de ITGβ4 e o risco de câncer. Pesquisa sobre câncer de mama 24, 98. https://doi.org/10.1186/s13058-022-01591-3
Liu, CS, Zhang, HB, Jiang, B., Yao, JM, Tao, Y., Xue, J., & Wen, AD (2012). Biodisponibilidade aprimorada e efeito cisticida de três preparações de óleo de mebendazol em camundongos infectados com cistos secundários de Echinococcus granulosus. Pesquisa em parasitologia, 111(3), 1205–1211. https://doi.org/10.1007/s00436-012-2954-2
Newton EE, Mueller LE, Treadwell SM, Morris CA, Machado HL. (2022) Alvos moleculares do câncer de mama triplo negativo: onde estamos? Cânceres (Basileia). https://doi.org/10.3390/cancers14030482.
Taherian-Fard A, Srihari S, Ragan MA. (2014) Classificação do câncer de mama: ligando mecanismos moleculares ao prognóstico da doença. Breve Bioinform.16:461–74.
Worsley, CM, Mayne, ES e Veale, RB (2016). Guerras dos clones: a evolução da resistência terapêutica no câncer. Evolução, medicina e saúde pública, 2016(1), 180–181. https://doi.org/10.1093/emph/eow015
Zhang L., Bochkur Dratver M., Yazal T., Dong K., Nguyen A., Yu G., Dao A., Bochkur Dratver M., Duhachek-Muggy S., Bhat K., et al. (2019). Mebendazol potencializa radioterapia no câncer de mama triplo-negativo. Internacional J. Radiat. Oncol. Biol. Física. 2019;103:195–207. doi: 10.1016/j.ijrobp.2018.08.046. – DOI – PMC – PubMed
Zhao J. (2016). Células-tronco cancerígenas e quimiorresistência: os mais inteligentes sobrevivem ao ataque. Farmacologia e Terapêutica, 160, 145–158. https://doi.org/10.1016/j.pharmthera.2016.02.008