Ana Maria Mihalcea, MD, PhD | substack.com/@anamihalceamdphd
Novo estudo mostra impacto significativo de nanoplásticos (NP) na função imunológica, causando toxicidade celular, inflamação, câncer e morte de glóbulos vermelhos. NP se acumula em órgãos.
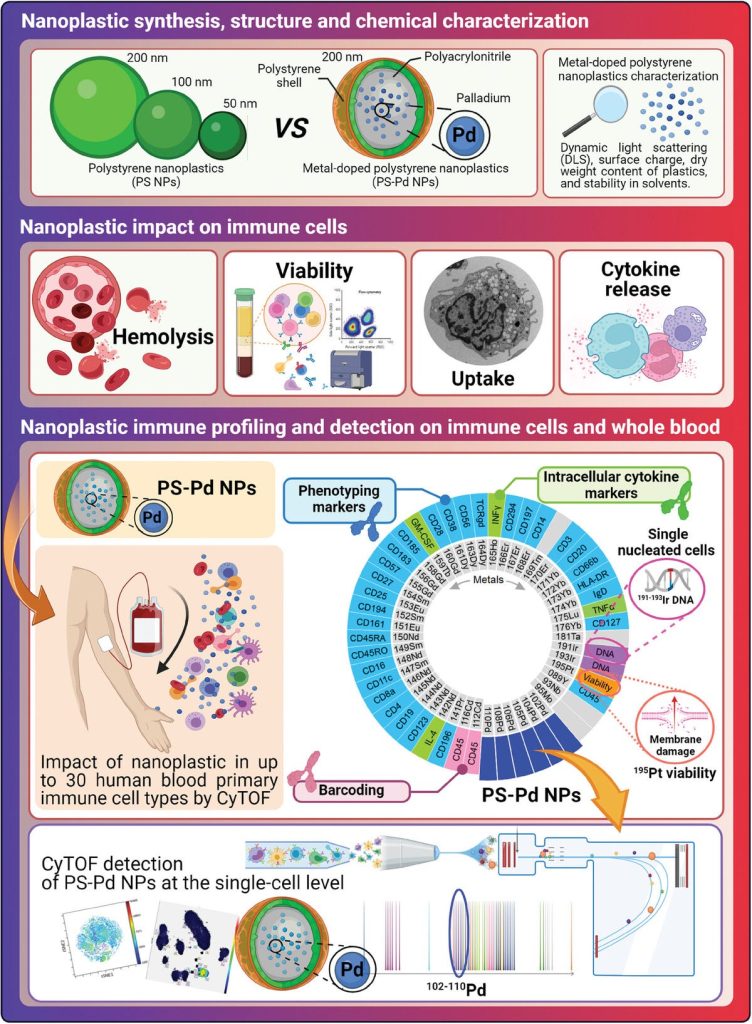
Um novo estudo publicado na Advanced Materials mostrou efeitos significativos dos nanoplásticos na função do sistema imunológico — aumento da resposta inflamatória.
A inflamação impulsiona todas as doenças do envelhecimento, causa acidez no corpo e diminui a voltagem elétrica celular. Se olharmos para o corpo de uma perspectiva eletrofisiológica, este estudo confirma o que temos visto na população humana – um processo de envelhecimento acelerado e disfunção imunológica, levando a problemas cardiovasculares, endócrinos e neurológicos acelerados e ao surgimento de cânceres turbo.
“Esses resultados demonstram que os NPs podem interagir, interferir e translocar em várias subpopulações de células imunes após a exposição. Experimentos de distribuição in vivo em camundongos confirmaram ainda mais seu acúmulo em células imunes dentro do fígado, sangue e baço, particularmente em monócitos, macrófagos e células dendríticas.”
Resumo
A crescente exposição a nanoplásticos (NPs) levanta preocupações significativas para a saúde humana, principalmente devido às suas potenciais propriedades bioacumulativas. Embora os NPs tenham sido detectados recentemente no sangue humano, suas interações com subtipos específicos de células imunes e seu impacto na regulação imune permanecem obscuros. Neste estudo de prova de conceito, NPs de poliestireno dopado com paládio modelo (NPs PS-Pd) são utilizados para permitir a detecção por citometria de massa de célula única (CyTOF). O impacto dependente do tamanho dos NPs de poliestireno carboxilato (50–200 nm) é investigado em 15 subpopulações primárias de células imunes usando CyTOF. Ao aproveitar a dopagem de Pd para detectar NPs PS-Pd, este trabalho avalia seu impacto nas células imunes humanas no nível de célula única após a exposição ao sangue. Este trabalho rastreia NPs de PS-Pd em 37 subpopulações primárias de células imunes do sangue humano, quantificando a contagem de átomos de paládio por célula por CyTOF enquanto avalia simultaneamente o impacto de NPs de PS-Pd na viabilidade, funcionalidade e absorção celular. Esses resultados demonstram que NPs podem interagir, interferir e translocar em várias subpopulações de células imunes após a exposição. Experimentos de distribuição in vivo em camundongos confirmaram ainda mais seu acúmulo em células imunes no fígado, sangue e baço, particularmente em monócitos, macrófagos e células dendríticas. Essas descobertas fornecem insights valiosos sobre o impacto de NPs na saúde humana.
O artigo cita um estudo de 2022 que encontrou nanopartículas de plástico no sangue humano. Surpresa! Após o lançamento da arma biológica da COVID19, encontramos plásticos de hidrogel de polímero no sangue de todos.
Descoberta e quantificação da poluição por partículas plásticas no sangue humano
Partículas plásticas são poluentes onipresentes no ambiente vivo e na cadeia alimentar, mas nenhum estudo até o momento relatou a exposição interna de partículas plásticas no sangue humano. O objetivo deste estudo foi desenvolver um método de amostragem e análise robusto e sensível com pirólise de tiro duplo – cromatografia gasosa/espectrometria de massa e aplicá-lo para medir partículas plásticas ≥700 nm em sangue total humano de 22 voluntários saudáveis. Quatro polímeros de alto volume de produção aplicados em plástico foram identificados e quantificados pela primeira vez no sangue. Polietileno tereftalato, polietileno e polímeros de estireno (um parâmetro de soma de poliestireno, poliestireno expandido, acetonitrila butadieno estireno etc.) foram os mais amplamente encontrados, seguidos por poli(metacrilato de metila). O polipropileno foi analisado, mas os valores estavam abaixo dos limites de quantificação. Neste estudo de um pequeno conjunto de doadores, a média da concentração quantificável de partículas plásticas no sangue foi de 1,6 µg/ml, mostrando uma primeira medição da concentração de massa do componente polimérico do plástico no sangue humano. Este estudo pioneiro de biomonitoramento humano demonstrou que as partículas plásticas são biodisponíveis para absorção na corrente sanguínea humana. Uma compreensão da exposição dessas substâncias em humanos e o risco associado a tal exposição é necessária para determinar se a exposição a partículas plásticas é ou não um risco à saúde pública.
Apenas lembrando a todos sobre as nanopartículas furtivas na patente da Moderna que contém polietileno, poliestireno e polimetacrilato:

Os cientistas analisaram os efeitos em 15 células diferentes do sistema imunológico e descobriram que a inflamação foi desencadeada, bem como a disfunção do sistema imunológico, inibindo a CAPACIDADE DE LUTAR CONTRA PATÓGENOS.
Usamos nanopartículas de poliestireno carboxilato (PS NPs), com diâmetros variando de 50 a 200 nm, para avaliar o impacto dependente do tamanho das NPs em quinze células imunes humanas primárias. Além disso, estudamos seus efeitos após exposição ao sangue por citometria de massa de célula única (CyTOF), uma tecnologia crucial e inovadora para decifrar o impacto biológico de vários agentes em profundidade.
Após a exposição humana, os NPs podem afetar as células imunes ao desencadear uma resposta inflamatória, levando à inflamação crônica e à desregulação imunológica. Além disso, os NPs podem interferir nas atividades das células imunes, como a fagocitose e a liberação de citocinas, comprometendo a capacidade do sistema imunológico de combater patógenos. Foi demonstrado que o tamanho dos NPs pode desempenhar um papel importante na determinação de seus efeitos tóxicos.
O tamanho importa, quanto maior, mais tóxico. Agora, lembre-se de que eles só olharam para a nanoescala – vejo filamentos de polímero que são centenas de vezes maiores do que uma hemácia (diâmetro de 5 micrômetros). Qual é a toxicidade relativa deles?
No geral, nossos dados demonstram que NPs PS maiores (200 nm) são mais eficazes na indução da produção de citocinas e ativação de células imunes, sugerindo um papel do tamanho das partículas em sua capacidade de afetar as funções das células imunes, em particular em células T e monócitos. Quanto maior o NP, maior a área de superfície, o que pode ser propício ao aumento da produção de citocinas, sugerindo que o tamanho é um fator crítico em seu impacto imunológico
As nanopartículas induzem a morte de glóbulos vermelhos chamada hemólise – vimos isso em muitos experimentos e eu mostrei isso em análises de sangue vivo. Lembra quando mostrei como os nano e microrobôs em anestésicos dentais matam glóbulos vermelhos em minutos?
Isto é o que o estudo mostrou:
Para avaliar a potencial atividade hemolítica de NPs, hemácias humanas foram expostas a 50 µg mL −1 de NPs de PS ou NPs de PS-Pd por 1 e 24 h (Figura S7d, Informações Complementares). NPs de PS-Pd induziram hemólise somente após 24 h, enquanto não observamos nenhuma liberação significativa de hemoglobina causada por NPs de PS.
Nesta parte do estudo, você pode ver que há muitas vias diferentes de como essas nanopartículas estão causando inflamação, bem como câncer como leucemia. Isso explicaria por que eu e outros médicos vemos turbo cânceres em não vacinados também agora, já que as nanopartículas de plástico são cancerígenas por meio de múltiplas vias.
Até esse ponto, a modulação de vários genes e proteínas ribossômicas também sugere aumento do estresse celular e possivelmente morte celular. Isso se alinha com a literatura existente, onde tratamentos que induzem estresse oxidativo demonstraram aumentar a regulação de genes e proteínas protetoras semelhantes. Curiosamente, entre as principais vias de regulação positiva identificadas pela análise da expressão gênica, encontramos a via do inflamossomo AIM2 (Figura 3c). O inflamossomo AIM2 é responsável por detectar DNA próprio e não próprio no citosol. Essa detecção inicia a montagem do inflamossomo e a liberação de IL-1β, promovendo a inflamação. Junto com os dados anteriores do ROS, isso sugere que o PS NP pode induzir danos às mitocôndrias, levando à liberação de DNA e à ativação do inflamossomo. Ao mesmo tempo, encontramos a regulação negativa da produção de ceramida mediada por TNFR1 e da sinalização de IL-38, indicando a supressão de mecanismos anti-inflamatórios, levando potencialmente a um aumento geral na inflamação e na produção de citocinas. A regulação positiva da via de resposta apoptótica regulada por SMAC-XIAP sugere um aumento na morte celular mediada, pois SMAC (Second Mitochondria-derived Activator of Caspases) promove a apoptose ao inibir XIAP (X-linked Inhibitor of Apoptosis Protein), facilitando assim a ativação da caspase, que também é necessária para a ativação da via do inflamossomo. Da mesma forma, a modulação do RUNX1 na via de diferenciação de células mieloides é conhecida por promover inflamação e uma maturação inadequada de monócitos que pode levar à Leucemia Mieloide Aguda (LMA). A análise proteômica confirmou a regulação de vias semelhantes, incluindo a transcrição regulada por RUNX1 de genes envolvidos na via de sinalização da interleucina (Figura 3d). A regulação positiva da atividade do apoptossomo é um complexo crucial na via de apoptose intrínseca. A regulação positiva de vias associadas ao HEXA defeituoso (mutações do gene HEXA que levam à doença de Tay-Sachs) que causam gangliosidose GM2 também implica aumento do estresse celular. Por outro lado, a regulação negativa da via de decaimento mediado por nonsense (NMD), que geralmente degrada transcrições de mRNA defeituosas, pode resultar no acúmulo de proteínas defeituosas, contribuindo para o estresse celular e a apoptose. Finalmente, a modulação das vias de oxidação de amina e geração de aldeído, como monoamina oxidases, MAOA e MAOB, destaca ainda mais que os NPs de PS induziram apoptose e formação de ROS por meio de mecanismos de estresse celular aprimorados (Figura 3d). Esses dados sugerem coletivamente que os NPs de PS impactam significativamente os monócitos induzindo dano mitocondrial, desencadeando ativação do inflamossomo, promovendo apoptose e aumentando o estresse celular, levando a uma resposta pró-inflamatória complexa.
Resumo:
Há evidências claras de que nanopartículas de polímero plástico afetam o sistema imunológico de todas as maneiras imagináveis e adversas. Inflamação e disfunção imunológica levam a todas as doenças do envelhecimento, bem como cânceres.