O grafeno, o nanomaterial de carbono 2D, é adequado para diversas aplicações, desde eletrônica e telecomunicações até energia e saúde. Apesar de suas enormes perspectivas tecnológicas e comerciais, suas interações com constituintes biológicos e ambientais ainda requerem um exame minucioso. Aqui, relatamos que o grafeno multicamadas puro se degrada na presença do peróxido de hidrogênio (H2O2), um composto onipresente e de ocorrência natural, em concentrações fisiologicamente e ambientalmente relevantes (1–10.000 × 10−6 M) em vários pontos de tempo (0–25h).
O grafeno, uma folha 2D composta de carbono hibridizado sp 2 possuindo propriedades elétricas, mecânicas, térmicas e ópticas excitantes, tem sido investigado como componentes facilitadores em células de combustível, sensores, fotocatálise, eletrônica, compósitos, biossensores elétricos e ópticos, drogas de entrega, engenharia de tecidos e sondas de imagem. Relatórios recentes preveem que o grafeno pode ultrapassar os nanotubos de carbono em aplicações comerciais. O desenvolvimento de potenciais tecnologias comerciais baseadas em grafeno para aplicações em ciências materiais e biomédicas levantou preocupações sobre seus efeitos de curto e longo prazo na saúde humana e no meio ambiente, e leva a várias investigações para avaliar esses efeitos.
Um atributo importante a ser examinado ao investigar o efeito do grafeno na saúde humana e no meio ambiente são suas propriedades de degradação biológica e ambiental. Vários estudos têm investigado a biodegradação de nanotubos de carbono, onde enzimas como a peroxidase de raiz forte (HRP) e a mieloperoxidase humana (hMPO) foram empregadas para catalisar a degradação oxidativa desses nanomateriais. Um estudo recente usou uma estratégia semelhante no óxido de grafeno e explora a atividade catalítica da enzima HRP. O H2O2 é um componente desse processo de degradação.
H2O2 é um composto onipresente de ocorrência natural e um forte agente oxidante, encontrado na chuva, nas águas superficiais e na biota. Sua concentração em fontes naturais de água foi determinada como sendo 1–7 × 10−3 M. Em células vivas normais, diversas vias celulares sintetizam H2O2 em concentrações rigidamente reguladas, variando entre 1 × 10−9 e 700 × 10−9 M. H2O2 concentrações estáveis >1 × 10−6 M causam estresse oxidativo e >1 × 10−3 M causam necrose. Assim, dada a presença generalizada de H2O2 no corpo e no ambiente, e o futuro impacto que o grafeno pode ter na saúde humana e no meio ambiente, estudos sistemáticos precisam ser realizados para investigar a interação química direta entre H2O2 e grafeno. Como primeiro passo, nesta comunicação, examinamos os efeitos de H2O2 em grafeno puro multicamadas em concentrações fisiologicamente e ambientalmente relevantes (1–10 000 × 10−6 M).
Grafeno multicamadas puro depositado em bolacha de níquel (tamanho da bolacha = 1 cm × 1 cm, Graphene Supermarket, Calverton, NY, EUA) ou diretamente em grades TEM foi colocado em placas de Petri e tratado com solução de H2O2 em concentrações de 1 × 10−6, 100 × 10−6 ou 10 000 × 10−6 M (n = 4 por grupo). O grafeno incubado com água destilada (DI) serviu como controle. Como as soluções de H2O2 gradualmente se deterioram, as soluções foram aspiradas a cada hora e trocadas por soluções novas. Os experimentos foram encerrados após 10 ou 25 h. Nesses pontos de tempo, as soluções foram completamente removidas e os substratos de grafeno foram secos ao ar. Amostras de grafeno antes (tempo t = 0 h) e depois do tratamento com H2O2 (tempo t = 10 e 25 h) foram examinadas com microscopia eletrônica de transmissão (TEM), microscopia de força atômica (AFM) e espectroscopia Raman confocal (excitação a laser de 532 milhas náuticas).
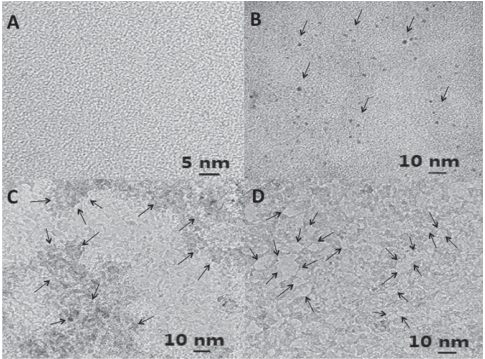
A Figura 1 mostra imagens TEM representativas de grades TEM revestidas com grafeno incubadas com várias concentrações de H2O2 por 10 h. A Figura 1 A mostra a folha de grafeno de controle incubada com água deionizada sem furos ou defeitos, e possui a rede hexagonal básica do grafeno, possuindo 0,142 nm de comprimento de ligação carbono-carbono, ocupando área de ≈ 0,17 nm2. Comparado com o grupo controle (Figura 1 A), o grafeno com tratamento de 1 × 10−6 M H2O2 após 5 h mostrou a presença de pequenos orifícios distribuídos aleatoriamente como visto na Figura 1 B (as setas apontam para poucos orifícios representativos). A distribuição do diâmetro dos furos no grafeno foi medida pela análise de múltiplas (n = 20) imagens TEM. A incubação do grafeno com 1 × 10−6 M H2O2 por 10 h resultou na formação de buracos variando de 1 a 15 nm de diâmetro (representando uma área de até 175 nm2). Assim, esses buracos visíveis indicam um “efeito de aglomerado”, ou seja, os buracos ou locais de defeitos são gerados inicialmente pelo ataque aleatório de H2O2 seguido pela atração progressiva de mais H2O2 para destruir as ligações carbono-carbono ao redor dos locais de defeitos iniciais. Esse efeito depende da concentração de H2O2 e é intensificado por concentrações mais altas de H2O2. Ao tratamento com 100 × 10−6 M H2O2, observou-se a formação de orifícios de maior tamanho (10–15 nm) (Figura 1 C). Além disso, a Figura 1 C também mostra a formação de regiões mais claras (poucas camadas de grafeno) e mais escuras (várias camadas de grafeno) indicando a degradação do grafeno multicamadas. A Figura 1 D mostra o grafeno após a incubação com 10 000 × 10−6 M H2O2. Locais com grandes defeitos (10-30 nm) e poucas camadas de grafeno foram observadas correspondendo à degradação da maioria das folhas de grafeno.
Figura 1. Imagens TEM representativas de grafeno multicamadas tratado com A) água deionizada, B) 1 × 10−6 M H2O2, C) 100 × 10−6 M H2O2 e D) 10 000 × 10−6 M H2O2 por 10 h. As setas em (B) indicam a formação de buracos nas folhas de grafeno, e as setas em (C) indicam a formação de regiões mais claras (poucas camadas de grafeno) e mais escuras (múltiplas camadas de grafeno) sugerindo a degradação do grafeno multicamadas. Deve-se notar que as setas em (B-D) apontam apenas para alguns orifícios representativos.
AFM foi realizada (usando um procedimento previamente descrito) para avaliar a topografia da superfície das folhas de grafeno antes e depois do tratamento com H2O2. As amostras foram incubadas com água desionizada e 10 000 × 10−6 M H2O2 durante 25 h. Folhas de grafeno imaculadas (Figura 2 A,C,E) pareciam lisas, sem quaisquer defeitos topográficos. Buracos distribuídos aleatoriamente em folhas de grafeno foram observados após incubação com H2O2 (Figura 2 B,D,E). O diâmetro dos orifícios variou de 5,3 a 13,5 nm. Comparado com a altura da folha única de grafeno (≈0,34 nm), a profundidade dos orifícios (9,4–13,5 nm, inserção da Figura 2 D) foi maior em várias dobras, sugerindo o ataque de H2O2 nas camadas internas do grafeno. Uma vez gerados os locais de defeitos superficiais, o H2O2 pode passar por esses locais de defeitos, atacando as ligações C-C subjacentes e acelerando a degradação do grafeno em concentrações mais altas de H2O2.
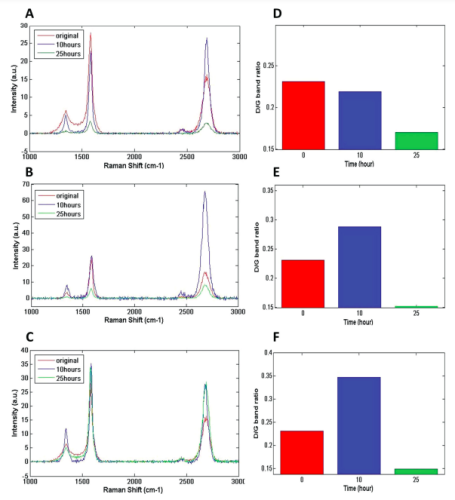
A espectroscopia Raman foi usada para caracterizar as amostras de grafeno antes e depois do tratamento com H2O2 em todos os momentos (Figura 3). A proporção das intensidades da banda D e da banda G (ID/IG) em todos os pontos de tempo antes e depois do tratamento com H2O2 são tabuladas na Tabela 1. A banda D que indica o grau de desordem no sistema de carbono sp 2 hidridizado foi observada entre 1335 e 1350 cm−1 , e a banda G, indicando estiramento do carbono grafítico, foi observada entre 1570 e 1580 cm−1. A Tabela 1 mostra a diminuição da intensidade das bandas D e G para todos os grupos tratados com várias concentrações de H2O2 por 25 h, sugerindo uma degradação estrutural gradativa do grafeno. Para os grupos tratados com 1 × 10−6 e 100 × 10−6 M H2O2, a razão ID/IG aumentou dentro de 10 h de incubação e diminuiu em momentos posteriores. O aumento na proporção ID/IG durante os pontos de tempo iniciais pode ser atribuído ao aumento no número de defeitos no grafeno e é consistente com relatórios anteriores sobre a degradação enzimática do grafeno. A diminuição na relação ID/IG em momentos posteriores pode ser atribuída à desintegração das múltiplas camadas de grafeno devido ao aumento progressivo nos tamanhos dos defeitos, expondo as camadas de grafeno primitivas subjacentes. Os espectros Raman dessas camadas de grafeno puro subjacentes teriam uma banda G intensa, reduzindo a relação ID/IG. Para o grupo tratado com 10 000 × 10−6 M H2O2, a razão ID/IG diminuiu progressivamente em todos os momentos, ao contrário dos grupos de tratamento 1 × 10−6 e 100 × 10−6 M H2O2, que mostraram um aumento inicial em a relação ID/IG nas primeiras 10 h. Após 25 h, ambas as bandas D e G quase desapareceram para o grupo de tratamento de 10.000 × 10-6 M H2O2.
A banda G’, uma característica do grafeno em camadas, foi observada em ≈ 2750 cm-1 para todos os grupos de tratamento. A intensidade da banda G’ aumentou durante as primeiras 10 h de tratamento com H2O2, diminuiu e tornou-se insignificante em momentos posteriores. A banda G’ tornou-se progressivamente estreita e deslocada para baixo em pontos de tempo crescentes. Vários relatórios têm mostrado a relação da banda G’ com o número de camadas de grafeno em que maior intensidade e um upshift da banda G’ corresponde ao aumento do número de camadas de grafeno. Neste estudo, à medida que a degradação progrediu, a diminuição na largura, intensidade e redução da banda G’ corresponde à degradação progressiva camada por camada do grafeno. Um fenômeno de degradação camada por camada foi observado durante a degradação de nanotubos de carbono de paredes múltiplas por HRP. Além disso, as diferenças na intensidade e largura do pico da banda G’ entre vários grupos de tratamento com H2O2 implicam na dependência da taxa de degradação do grafeno na concentração de peróxido de hidrogênio, ou seja, o grafeno tratado com 1 × 10−6 M H2O2 pode degradar em um ritmo mais lento taxa em comparação com o tratamento com 10 000 × 10−6 M H2O2.
Figura 2. Imagens AFM representativas de grafeno multicamadas em wafer de Ni. A,C,E) são varreduras topográficas de amostras de grafeno intocadas (incubadas com água DI) e B,D,E) são grafenos após 25 h de tratamento com H2O2 (10 000 × 10−6 M). As inserções nas imagens C e D correspondem ao perfil de altura da linha. As imagens E e F são representações 3D das imagens C e D, respectivamente.
Os resultados acima, tomados em conjunto, indicam claramente a degradação do grafeno puro multicamadas em uma ampla gama de concentrações de H2O2 encontradas em sistemas vivos e no meio ambiente. Estudos anteriores relatam que íons metálicos como níquel (Ni), ferro (Fe) e cobre (Cu) podem catalisar a degradação de H2O2 para formar radicais hidroxila reativos por meio da reação de Haber-Weiss. Substratos ou catalisadores à base de Ni, Fe ou Cu são usados para a síntese de grafeno usando o método de deposição química de vapor. Assim, neste estudo, a presença de traços de Ni usados durante a síntese CVD do grafeno pode estar catalisando a degradação do grafeno durante o tratamento com H2O2. Os resultados também indicam que a taxa de degradação do grafeno é dependente da concentração de exposição ao H2O2; O aumento da concentração acelera a degradação do grafeno. Os orifícios visíveis indicam um “efeito de aglomerado”, ou seja, os orifícios ou locais de defeito são gerados inicialmente pelo ataque aleatório de H2O2 seguido pela atração progressiva de mais H2O2 para destruir a ligação carbono-carbono em torno dos locais de defeito iniciais. Além disso, a temperatura da reação também pode influenciar a taxa de degradação. Estudos adicionais são necessários e atualmente em andamento para testar a hipótese acima e fornecer uma melhor compreensão do mecanismo químico da degradação do grafeno mediada por H2O2 (interação da concentração de H2O2, temperatura de reação e presença de íons metálicos).
Uma grande variedade de enzimas peroxidase catalíticas, como MPO, HRP e lignina peroxidase (LiP), estão presentes no corpo ou no ambiente. Vários estudos investigaram os efeitos de enzimas como HRP e hMPO na degradação de nanotubos de carbono de paredes simples e múltiplas. Um estudo recente demonstrou a degradação do óxido de grafeno na presença de HRP. Esses estudos indicam que a degradação enzimática depende da funcionalização da superfície dos nanomateriais de carbono e requer etapas de pré-tratamento, que incluem exposição a ácidos fortes e oxidantes antes da degradação enzimática. Além disso, foi relatado que esse processo de degradação é eficaz após a exposição contínua de nanomateriais de carbono a enzimas e H2O2. Assim, as enzimas peroxidases certamente poderiam acelerar a degradação do grafeno na presença de H2O2.
No entanto, essas enzimas são encontradas principalmente na proximidade de certas células animais (MPO é secretada por células inflamatórias – neutrófilos), células vegetais (HRP está presente na raiz da planta de rabanete) ou fungos (LiP é encontrado em fungos como como Phanerochaete chrysosporium). O H2O2, por outro lado, não está restrito a esses bioorganismos, mas é onipresente nas células eucarióticas e nos recursos naturais (água doce e do mar). Nossos resultados sugerem fortemente que o mecanismo alternativo de degradação na presença de H2O2 em concentrações fisiologicamente e ambientalmente relevantes (1–10 000 × 10−6 M) pode iniciar e degradar grafeno puro de uma e múltiplas camadas.
As limitações do estudo acima são: enquanto as concentrações de H2O2 mimetizam aquelas encontradas em condições fisiológicas e ambientais, as condições experimentais controladas permitem que todo o H2O2 disponível interaja com o grafeno; outros processos redox concorrentes em sistemas biológicos ou ambientes que requerem H2O2 estavam ausentes. A presença desses processos concorrentes prejudicará a taxa de degradação. Os estudos foram realizados em folhas multicamadas de grafeno puro. Assim, este estudo fornece apenas informações sobre o efeito de degradação da superfície do H2O2. A degradação em massa na quantidade macroscópica de agregados de grafeno na presença de H2O2 ainda precisa ser determinada.