Ross M Kedl, Elena WY Hsieh, Thomas E Morrison, Gabriela Samayoa-Reyes, Siobhan Flaherty, Conner L Jackson, Rosemary Rochford
Resumo
Partículas infecciosas podem ser compartilhadas por meio de aerossóis e gotículas formadas como resultado da respiração normal. Não foi investigado se Abs dentro dos fluidos nasais/orais podem ser compartilhados de forma semelhante entre hospedeiros. As circunstâncias da pandemia de SARS-CoV-2 facilitaram uma oportunidade única de examinar completamente essa ideia provocativa. Os dados que mostramos de swabs nasais humanos fornecem evidências da transferência de Abs por aerossol entre hospedeiros imunes e não imunes.
Introdução
As vacinas contra SARS-CoV-2 mantiveram eficácia notável contra doenças graves e morte em vacinados, independentemente do surgimento de variantes, incluindo a Omicron. Menos apreciados do que a imunidade sistêmica gerada pelas vacinas são os altos níveis de Ab (IgG e IgA) encontrados na cavidade nasal e na saliva dos vacinados. Esse resultado é encontrado tanto em humanos quanto em primatas, e em resposta a vacinas baseadas em mRNA e proteína (Ref. 2 e GR Nahass, RE Salomon-Shulman, G. Blacker, K. Haider, R. Brotherton, K. Teague, YY Yiu, RE Brewer, SD Galloway, P. Hansen, manuscrito publicado em bioRxiv, DOI: 10.1101/2021.08.22.21262168). A transmissão respiratória da infecção viral é prova de que os constituintes da cavidade oral/nasal podem ser comunicados por meio de aerossóis e/ou gotículas respiratórias. Dessa forma, seria lógico supor que o Ab presente no ambiente oral/nasal também possa ser aerossolizado até certo ponto.
Materiais e métodos
Imunoensaio de microesferas multiplexadas
Um imunoensaio de microesferas multiplexadas (MMI) foi desenvolvido usando microesferas LEGENDplex carboxiladas BioLegend para quantificar simultaneamente IgG e IgA contra o domínio de ligação ao receptor de espícula (RBD) e o nucleocapsídeo da cepa Wuhan do SARS-CoV-2 (Sino Biological, RBD, catálogo nº 40150-D002; nucleocapsídeo, catálogo nº 40143-MM08) e toxoide tetânico (TT) (MilliporeSigma, catálogo nº 582231) como controle positivo. As esferas conjugadas com BSA foram usadas como controle negativo. A validação da conjugação de proteína-esfera RBD e TT foi realizada por coloração com um mAb anti-RBD (humano quimérico, D002, Sino Biological, Wayne, PA) ou mAb anti-TT (mouse Ab, Jackson ImmunoResearch, West Grove, PA), respectivamente. As esferas foram misturadas em proporções iguais (∼2000 cada esfera/poço de amostra) e incubadas com soro, saliva, eluatos de máscara ou amostras de swab nasal em tampão de armazenamento/corrida (PBS contendo 0,01% de Tween 20, 0,05% de NaN 3 e 0,1% de BSA) e agitadas em uma placa agitadora por 60 min em temperatura ambiente e então lavadas. A IgG ligada foi detectada por anti-IgG humana secundária-biotina (diluição 1:3000) (SouthernBiotech, Birmingham, AL), seguida pela adição de estreptavidina-PE (diluição 1:1000) (BD Biosciences, San Jose, CA) e anti-F(ab′) 2 IgA-FITC humana (SouthernBiotech, Birmingham, AL). A intensidade de fluorescência média geométrica (gMFI) da IgG/IgA para cada amostra e diluição foi capturada com um citômetro de fluxo CytoFLEX S (Beckman Coulter) e analisada com FlowJo (versão 10.7.1; BD Biosciences). O Prism (versão 8.4.3, GraphPad) foi usado para plotar os dados.
Aquisição e análise de amostras humanas
Soro humano, saliva e swabs nasais foram obtidos (aprovação do Institutional Review Board n.º 20-1279). Máscaras cirúrgicas foram doadas anonimamente por trabalhadores de laboratório no final de um dia de trabalho. Punções (quatro) foram retiradas do meio de cada máscara e o Ab foi eluído conforme descrito anteriormente. Resumidamente, um punção manual de 6 mm foi usado para fazer punções da máscara, coletadas em uma placa de cultura de células de 24 poços com 500 μl de um tampão de eluição (PBS contendo 0,05% de Tween 20 e 0,08% de NaN3 ) , então colocadas em um agitador de plataforma por 2 h em temperatura ambiente. A eluição foi coletada e armazenada a -80 °C até o uso no MMI. Os swabs nasais foram obtidos por amostragem de conveniência de pais e filhos no centro de vacinação Colorado Tri-County em Aurora, CO, que estavam participando de consultas de vacinação, não limitadas ao SARS-CoV-2. Ab das pontas de swab foi eluído conforme descrito para manchas de sangue seco. Os valores de IgA e IgG transformados em logaritmo das amostras das crianças foram modelados usando regressão linear com uma única covariável binária correspondente a níveis altos ou baixos de Ab de seus pais. Como a distribuição dos dados para gMFI de IgG adulta era unimodal e fortemente enviesada para a direita, um procedimento de bootstrapping ajudou a identificar um corte que separava uma população “baixa” normalmente distribuída (∼66% das amostras) de uma população “alta” (∼33%) de outliers. A distribuição resultante de valores baixos foi normalmente distribuída, sem enviesamento e curtose razoável. Gráficos residuais foram usados para verificar violações de suposições de regressão linear, e um teste de soma de postos de Wilcoxon foi conduzido quando as suposições foram violadas. Um modelo linear de efeitos mistos foi avaliado para garantir que a correlação dentro de uma família não contribuísse significativamente para os dados ou alterasse as conclusões tiradas do modelo de regressão linear de efeito fixo. A citometria foi realizada usando um citômetro Beckman Coulter CytoFLEX e analisada usando o software FlowJo versão 10 (Tree Star). As análises estatísticas foram conduzidas usando R (versão 4.0.2).
Disponibilidade de dados
Todos os materiais, dados e protocolos associados estarão disponíveis aos leitores mediante solicitação e sem qualificações indevidas.
Resultados
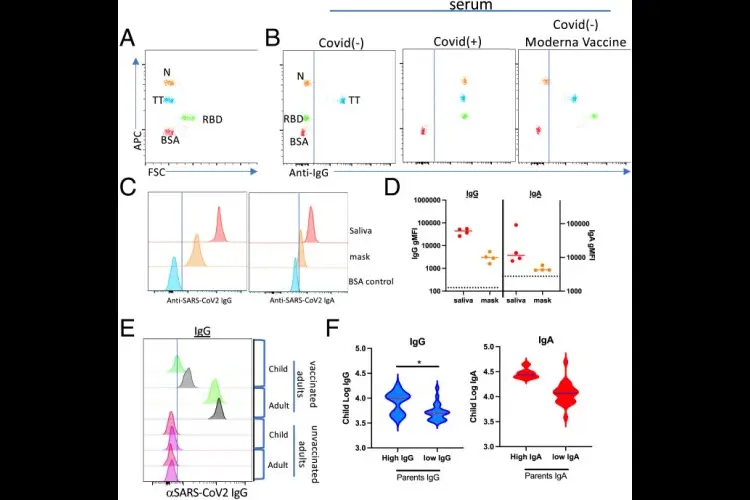
Os mandatos estendidos para o uso de máscaras em ambientes sociais e de trabalho forneceram uma oportunidade única para avaliar a possibilidade de expiração de Ab aerossolizados de indivíduos vacinados. Utilizando um MMI baseado em citometria de fluxo para detectar Abs específicos para SARS-CoV-2 (Fig. 1A, 1B) e um método usado anteriormente para eluir Ab de manchas de sangue seco reidratadas, identificamos Abs específicos para anti-SARS-CoV-2 eluídos de máscaras cirúrgicas que foram usadas por 1 dia de trabalho por membros vacinados do laboratório. Consistente com os resultados relatados por outros, identificamos IgG e IgA na saliva de indivíduos vacinados (Fig. 1C, 1D). Portanto, não foi surpreendente detectar IgG e IgA após a eluição de máscaras faciais (Fig. 1C, 1D).
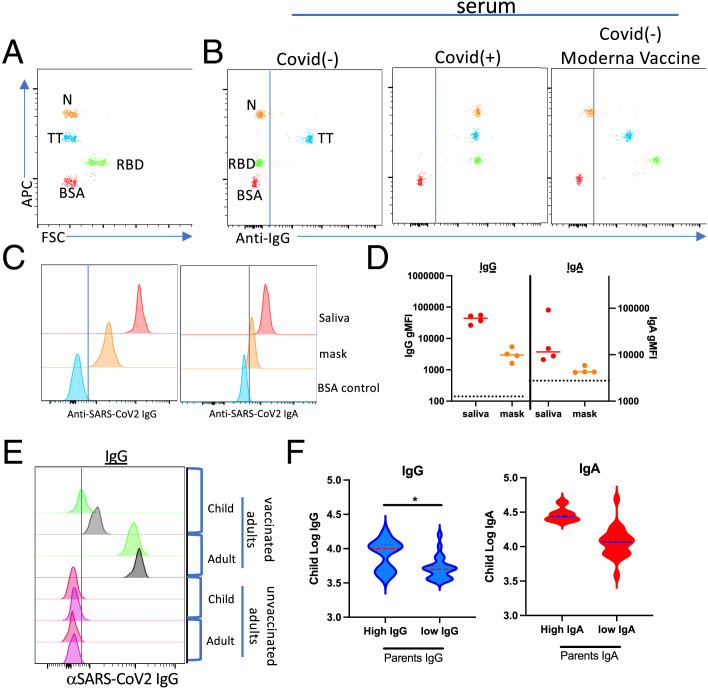
Dadas essas observações, levantamos a hipótese de que a transferência de gotículas/Ab aerossolizados pode ocorrer entre indivíduos, assim como partículas de vírus em gotículas/aerossolizados podem ser trocadas pela mesma rota. Para avaliar essa hipótese, obtivemos swabs nasais de crianças que viviam em domicílios nos quais os pais ou familiares tinham graus variados de imunidade específica para SARS-CoV-2, incluindo aquelas não vacinadas (anti-RBD–negativo, anti-proteína do nucleocapsídeo [N]–negativo), vacinadas (anti-RBD–positivo, anti-N–negativo) e COVID-19+ (anti-RBD–positivo, anti-N–positivo). Todas as crianças avaliadas foram presumidas como COVID-19–negativas com base em serem negativas para Abs anti-N. A comparação inicial de swabs nasais adquiridos de crianças que vivem em domicílios vacinados revelou IgG específica para SARS-CoV-2 prontamente detectável (Fig. 1E), especialmente quando comparado com o déficit completo de Ab específico para SARS-CoV-2 detectado nos poucos swabs nasais que obtivemos de crianças em domicílios não vacinados. Usamos a variação nos níveis de IgG intranasal dos pais como base de estratificação em todas as amostras de crianças. Gráficos de densidade de dados brutos e transformados em log de 34 pares adulto/criança foram usados para estabelecer pontos de corte de Ab para níveis altos versus baixos de Ab intranasal parental. A avaliação de amostras dessa forma revelou que IgG intranasal alta em pais vacinados foi significativamente associada ( p = 0,01) com um aumento de 0,38 nos gMFIs de IgG intranasal transformados em log em uma criança do mesmo domicílio (Fig. 1F). Essa relação positiva significativa foi observada usando análise paramétrica ou não paramétrica, e os ajustes para a correlação dentro do domicílio não alteraram a conclusão. Embora não estatisticamente significativa, uma tendência semelhante de IgA elevada foi encontrada nas mesmas amostras.
Discussão
A interpretação mais simples dos nossos resultados é que 1) a transmissão de Ab por aerossol pode ocorrer e que 2) a propensão para essa transferência é, sem surpresa, diretamente relacionada à quantidade de Ab nasal/oral encontrada entre aqueles na população que possuem imunidade. Ainda não encontramos uma interpretação igualmente parcimoniosa, embora isso não signifique que não exista. O conceito de imunidade de rebanho é um inquilino central das campanhas de vacinação de saúde pública. O bloqueio aberto da infecção, bem como uma redução na transmissão viral a jusante de uma infecção de ruptura são mecanismos conceituais amplamente aceitos pelos quais a imunidade induzida pela vacinação em indivíduos específicos protege membros não imunes da comunidade. Com isso em mente, é lógico que a transmissão de Abs por aerossol também pode contribuir para a proteção do hospedeiro e representar um mecanismo totalmente não reconhecido pelo qual a proteção imunológica passiva pode ser comunicada.
Como não foi observada reatividade cruzada entre proteínas spike do coronavírus sazonal e o RBD do SARS-CoV-2, não acreditamos que nossos resultados tenham sido indevidamente influenciados pela exposição prévia dos indivíduos ao coronavírus sazonal. Embora haja um pequeno grau de reatividade cruzada entre os domínios S2 do SARS-CoV-2 e a cepa sazonal OC43, isso não se estende ao domínio S1 ou ao RBD mais limitado. Se isso fosse verdade, é discutível que o curso da pandemia teria sido substancialmente alterado para melhor.
Infelizmente, a dificuldade em recrutar participantes de domicílios não vacinados em conjunto com a disponibilidade das vacinas para crianças menores de 5 anos tornou a aquisição contínua de amostras insustentável. Como tal, não fomos capazes de determinar se a transferência de IgA por aerossol poderia atingir significância estatística a partir do aumento da avaliação da amostra, nem fomos capazes de elaborar qualquer ensaio adequado para determinar a relevância biológica da transferência de IgG por aerossol observada. No entanto, se a transferência de Ab media a proteção do hospedeiro será uma função da exposição, e parece razoável sugerir, todas as coisas sendo iguais, que qualquer quantidade de transferência de Ab seria útil para o hospedeiro receptor. Com os benefícios documentados da vacinação parental na redução do risco de infecção em crianças não vacinadas na mesma casa, é tentador especular que a transferência de Ab mediada por aerossol pode ter possivelmente contribuído para as descobertas relatadas. Parece provável que os swabs nasais coletados originalmente para monitorar a transmissão do SARS-CoV-2 neste estudo possam ser reutilizados para examinar IgG e IgA específicos do SARS-CoV-2 em adultos vacinados, bem como em familiares não infectados, potencialmente fornecendo o poder estatístico necessário para validar as conclusões tiradas no estudo atual.
EVIDÊNCIAS DE TRANSFERÊNCIA DE AEROSSOL DE IMUNIDADE HUMORAL ESPECÍFICA PARA SARS-COV-2
Fonte: https://pmc.ncbi.nlm.nih.gov/articles/PMC10579981/