Como tantas flores malévolas, a proteína Spike “floresce” inflamação nos órgãos, levando a danos e morte.
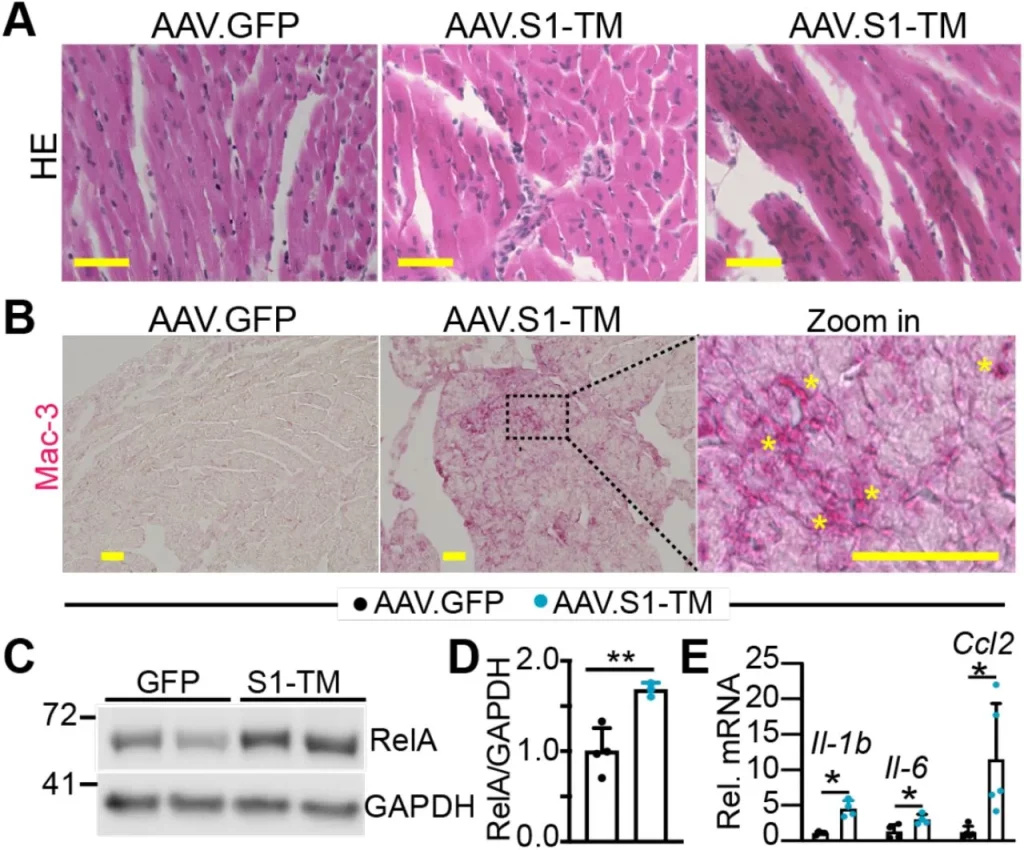
S1-TM induz inflamação cardíaca.
A. Miocárdio corado com HE. Barra de escala = 50 μm. B. Coloração imuno-histoquímica de Mac-3 no miocárdio. Sistema de detecção baseado em fosfatase alcalina foi usado para visualizar células positivas para Mac-3. Na imagem ampliada, estrelas amarelas indicam aglomerados de macrófagos. Barra de escala = 50 μm. C. Imunoblot de RelA. D. Quantificação densitométrica de RelA. Os níveis de proteína RelA foram normalizados para GAPDH. N=3-4. E. Medição de qRT-PCR de Il-1b, Il-6 e Ccl2. N=4-5. D,E, teste t de Student, *, P<0,05; **, P<0,01.
Expressão seletiva da subunidade S1 da proteína Spike do SARS-CoV-2 em cardiomiócitos induz hipertrofia cardíaca em camundongos
https://www.biorxiv.org/content/10.1101/2021.06.20.448993v1.full
Por favor, estude a imagem acima com atenção.
Agora, por favor, estude este.
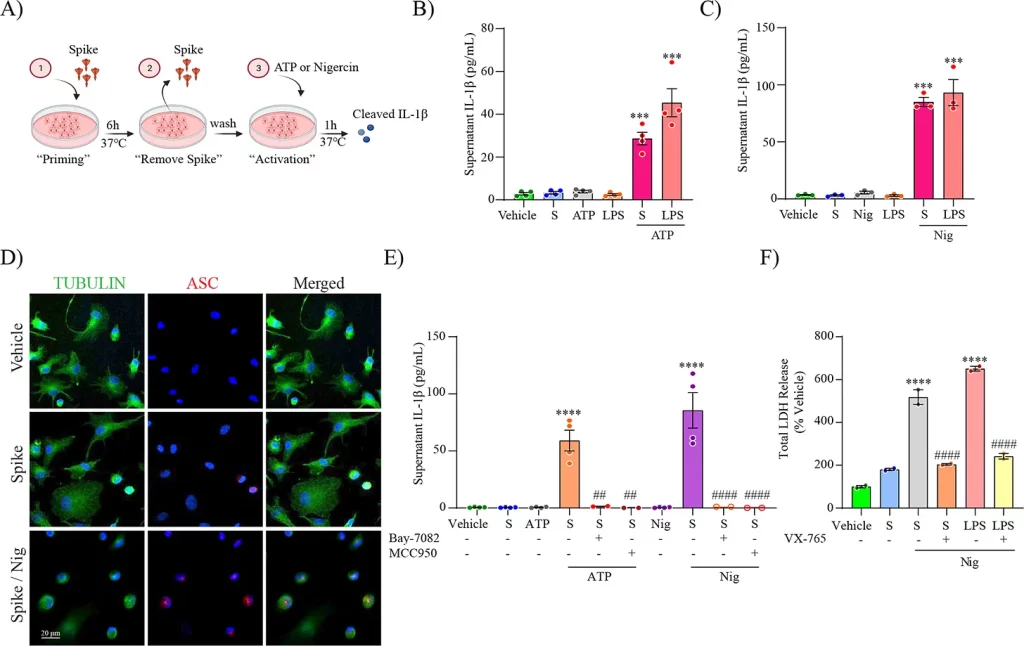
A proteína spike do SARS-CoV-2 prepara o inflamassoma NLRP3 por meio do NF-kB.
Representação esquemática para experimentos de preparação de pico (6 h) seguidos de ativação de ATP ou Nigericina (Nig) (1 h) (A). Nível de IL-1β secretado em MDMi não preparado ou preparado com S-clamp (S; 50 μg 6 h) seguido de ativação com ATP (5 mM, 1 h) em (B) ou Nigericina (Nig; 10 μM, 1 h) em (C). Em ambos os casos, células preparadas com LPS foram usadas como controle positivo (200 ng/ml 3 h). Coloração por imunofluorescência de MDMi preparado com veículo ou S-clamp (S; 50 μg 6 h), ativado com Nigericina (Nig; 10 μM, 1 h) mostrando tubulina (verde) e a formação de uma mancha ASC característica do inflamossomo (vermelha) são mostradas em (D). Barra de escala 20 μm. A secreção de IL-1β mediada por ATP e Nigericina (sobrenadante) em MDMIs veículo (não tratado) ou preparados com S-clamp expostos a ATP (5 mM, 1 h) ou Nigericina (Nig; 10 μM, 1 h) na presença ou ausência de Bay 11-7082 (3 μM) ou MCC950 (10 μM) são mostrados em (E). Ensaio de liberação de lactato desidrogenase (LDH) para quantificação de piroptose dependente de caspase-1 em células preparadas com S-clamp (S; 50 μg 6 h) ativadas com Nigericina (Nig; 10 μM, 1 h) em (F). LPS-Nigericina e VX-765 (20 μM) foram usados como controles positivos. Os dados são médias ± SEM de pelo menos 3 doadores independentes. ***P < 0,001 e ****P < 0,0001 pela análise de variância unidirecional (ANOVA) com teste post hoc de Tukey.
O SARS-CoV-2 impulsiona a ativação do inflamossomo NLRP3 na microglia humana por meio da proteína spike
https://www.nature.com/articles/s41380-022-01831-0
Próximo.
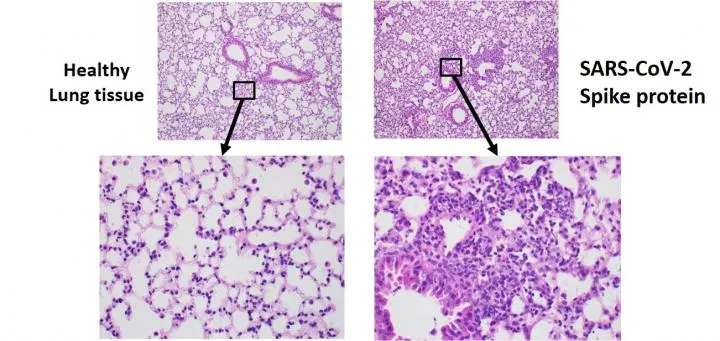
Usando um modelo de camundongo recém-desenvolvido, os pesquisadores descobriram que a exposição à proteína spike do SARS-CoV-2 sozinha foi suficiente para induzir sintomas semelhantes aos da COVID-19, incluindo inflamação grave nos pulmões. As imagens da esquerda mostram tecido pulmonar saudável de camundongo, enquanto as imagens da direita mostram tecido de pulmões de camundongo expostos à proteína spike.
A proteína spike do SARS-CoV-2 sozinha pode causar danos pulmonares
https://www.eurekalert.org/news-releases/490426
E…
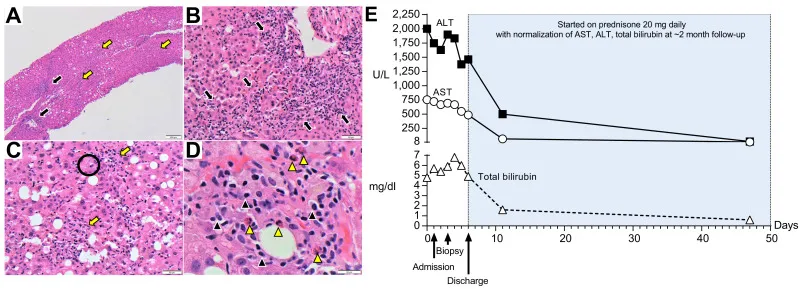
(A) Baixa ampliação (40x) mostra hepatite pan-lobular (setas pretas: inflamação portal e setas amarelas: inflamação lobular). (B) Imagens de média ampliação (200x) mostram um trato portal com um intenso infiltrado linfoplasmocitário apagando a interface com formação de roseta e (C) atividade lobular com necrose de hepatócitos espalhados (círculo preto: corpos acidófilos). (D) Em alta ampliação (600x), a inflamação consiste principalmente de linfócitos com células plasmáticas (pontas de seta pretas) e eosinófilos (pontas de seta amarelas). (E) Tendências de ALT plasmática, AST e bilirrubina total ao longo do tempo.
Hepatite autoimune se desenvolvendo após a vacina contra a doença do coronavírus 2019 (COVID-19): Causalidade ou casualidade?
https://www.journal-of-hepatology.eu/article/S0168-8278(21)00237-3/fulltext
Continuando.
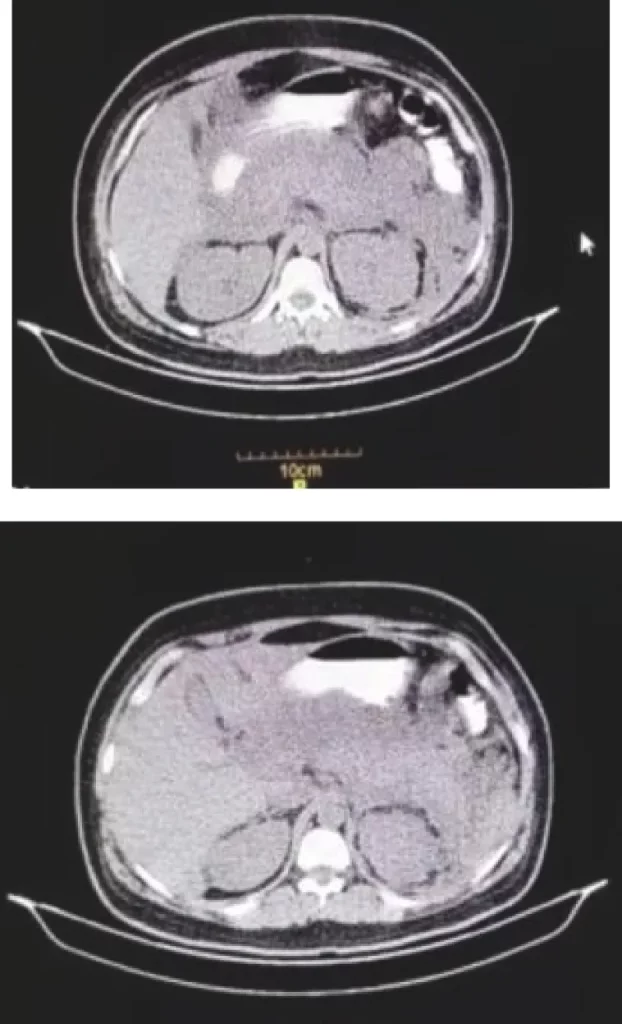
Tomografia computadorizada (TC) do abdome. Foi observado aumento homogêneo do pâncreas, extensa gordura peripancreática e fluido peripancreático.
Pancreatite aguda após vacina contra COVID-19: relato de caso e breve revisão da literatura https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9840226/
Mas é claro.
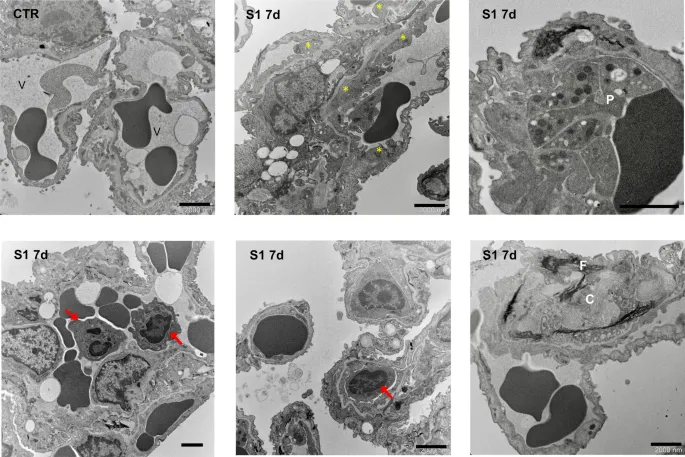
A injeção de S1 induz alterações ultraestruturais endoteliais no tecido pulmonar de camundongos hACE2-KI. Análise ultraestrutural do tecido alveolar pulmonar de camundongos CTR e S1 injetados em 7d. Em camundongos CTR, células endoteliais vasculares finas formam o revestimento interno do capilar alveolar (V). Camundongos injetados com S1 em 7d mostram áreas de espessamento de células endoteliais (asteriscos amarelos), associadas a plaquetas ativadas (P), acúmulo de células inflamatórias (setas vermelhas), incluindo neutrófilos e monócitos, e material com aspecto fibrilar (F) e deposição de colágeno (C). Barras de escala: 2000 nm.
A proteína spike do SARS-CoV-2 induz disfunção das células endoteliais pulmonares e tromboinflamação dependendo da sinalização do receptor C3a/C3a
https://www.nature.com/articles/s41598-023-38382-5
Eu poderia continuar, mas tenho certeza de que você não vê necessidade.
Agora. Vamos ler alguns parágrafos juntos, tudo bem?
Esclerose múltipla (EM) é uma doença neurológica crônica que é caracterizada por inflamação irregular, gliose e desmielinização dentro do sistema nervoso central (SNC). É a terceira causa mais comum de incapacidade em adultos entre 18 e 50 anos de idade.
Dor crônica na esclerose múltipla: prevalência, características e impacto na qualidade de vida em uma coorte comunitária australiana
https://www.sciencedirect.com/science/article/pii/S1526590007006396
A DII abrange um grupo de distúrbios inflamatórios crônicos, idiopáticos e recorrentes que afetam o trato gastrointestinal. As duas formas primárias de DII são a doença de Crohn (DC) e a colite ulcerativa (CU)40–42. As manifestações clínicas da DII variam dependendo da localização e da gravidade da inflamação no trato gastrointestinal. A DC é caracterizada por inflamação irregular que pode afetar toda a espessura da parede intestinal ao longo dos intestinos delgado e grosso42–45. Pode haver áreas de tecido saudável entre as seções inflamadas (lesões saltadas).
Desvendando a relação entre periodontite e doença inflamatória intestinal: desafios e perspectivas
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10462160/
Colangite esclerosante primária (CEP) é uma inflamação irregular, fibrose e estenoses dos ductos biliares sem causa conhecida.
Colangite esclerosante primária (CEP)
A fibrose e a atrofia pancreática foram classificadas de acordo com o sistema de pontuação de Klöppel e Maillet [21]. A fibrose perilobular foi definida como a presença de tecido conjuntivo nos espaços interlobulares [21]. A fibrose intralobular foi definida como a presença de tecido conjuntivo que se estende da fibrose perilobular aos lóbulos acinares com substituição fibrosa das células acinares [21]. A fibrose foi classificada como uma extensão da fibrose para os lóbulos acinares com substituição fibrosa parcial (leve: 10–40%; moderada: 40–80%) ou (quase) completa (grave: 80–100%) das células acinares. A atrofia acinar foi definida como a destruição das células acinares e substituição da fibrose. A atrofia acinar das lâminas de espécimes tumorais foi classificada de forma semelhante da seguinte forma: substituição fibrosa parcial (leve: 10–40%; moderada: 40–80%) ou (quase) completa (grave: 80–100%) das células acinares. A inflamação crônica foi classificada como leve, moderada e grave de acordo com o número de células inflamatórias mononucleares (ver Figuras Adicionais 1 e 2). A inflamação crônica leve e moderada foi caracterizada por inflamação irregular. Além disso, a inflamação crônica moderada exibiu maior número de células inflamatórias mononucleares do que a inflamação crônica leve. Um padrão difuso de inflamação foi evidente na inflamação crônica grave. As alterações do ducto incluíram a distorção dos ductos, fibrose periductal, presença de tampões de proteína, cálculos, destruição epitelial, inflamação periductal e neoplasia intraepitelial pancreática (PanIN) [21].
Fibrose pancreática, atrofia acinar e inflamação crônica em espécimes cirúrgicos associados à sobrevivência em pacientes com adenocarcinoma ductal pancreático ressecável https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8721973/
E isso é só a ponta do iceberg. Todos os itens acima estão associados à exposição pós-COVID/Spike Protein.
Como um protagonista maligno que invade a Parábola do Semeador, o SARS-CoV-2 (ou mRNA) lança sua Proteína Spike para longe e para longe. Em alguns (muitos) lugares, ela cria raízes e então, como mencionado acima, prossegue para “florescer” em manchas de inflamação. Danificando e destruindo órgãos e tecidos.
Talvez a manifestação mais alarmante seja a dos incidentes de Miocardite.
Autópsias revelaram inflamação irregular sugerindo que morte arrítmica súbita poderia ter ocorrido devido a uma arritmia ventricular reentrante culminando em morte cardíaca súbita. Os autores nesses casos concluíram que a causa da morte foi miocardite induzida pela vacina COVID-19.
Resultados de autópsia em casos de miocardite fatal induzida pela vacina COVID-19
https://onlinelibrary.wiley.com/doi/10.1002/ehf2.14680
Obviamente, o coração pode exibir os efeitos mais dramáticos e imediatos. Mas meu ponto é que há outros órgãos, outros sistemas que estão sendo igualmente afetados pela inflamação da Proteína Spike. É como o clássico filme de terror The Blob . Áreas de inflamação surgem, se desenvolvem, muito provavelmente se fundem.
No entanto, há esperança. Podemos impedir que o Spike se ligue. Podemos reduzir os níveis de inflamação. Podemos degradar seus microcoágulos. Podemos proteger nosso endotélio, bem como outros órgãos. O Spike é um oportunista supremo. Não dê a ele uma chance.
Fonte: https://wmcresearch.substack.com/p/systemic-inflammation-the-raison