Pesquisador: Walter Castanha
1 EbMCsquared CIC, 11 Laura Place, Bath BA2 4BL, Reino Unido
2 Center for Biophysical Osteopathy, Am Wegweiser 27, 55232 Alzey, Alemanha
3 Front Line COVID-19 Critical Care Alliance (FLCCC), 2001 L St. NW Suite 500, Washington, DC 20036, EUA
(Este artigo científico pertence à Edição Especial Avanços Recentes em Antivirais para Vírus Emergentes 2.0)
Abstrair
Na esteira da crise COVID-19, surgiu a necessidade de prevenir e tratar duas condições relacionadas, a lesão da vacina COVID-19 e a COVID-19 longa, ambas as quais podem rastrear pelo menos parte de sua etiologia para a proteína spike, que pode causar danos através de vários mecanismos. Um mecanismo significativo do dano é vascular, e é mediado pela proteína spike, um elemento comum da doença COVID-19, e está relacionado ao recebimento de uma vacina COVID-19. Dado o número significativo de pessoas que experimentam essas duas condições relacionadas, é imperativo desenvolver protocolos de tratamento, bem como considerar a diversidade de pessoas que experimentam COVID-19 longo e lesões vacinais. Esta revisão resume as opções de tratamento conhecidas para COVID-19 longo e lesão vacinal, seus mecanismos, e sua base probatória.
Palavras-chave:
COVID longa; lesão da vacina COVID-19; proteína spike; trombose; inflamação; medicação reaproveitada; autofagia
1. Introdução
De acordo com os dados disponíveis, até 30 de setembro de 2022, 68% da população mundial tinha recebido pelo menos uma dose da vacina COVID-19, e 12,74 bilhões de doses tinham sido administradas [1]. As vacinas mais comumente administradas foram Comirnaty (Pfizer/BioNTech), Covishield (Astrazeneca), CoronaVac (Sinovac), Spikevax (Moderna) e Jcovden (Johnson Johnson) [2]. Destes, aproximadamente 30% das doses produzidas até 22 de janeiro de 2022 foram na forma de uma nova vacina com um mRNA sintético N1-metil-pseudoiridinilado encapsulado em uma nanopartícula lipídica (LNP) [3].
LNPs são uma tecnologia nova que não foi usada na entrega de vacinas até a autorização de uso emergencial (EUA) das vacinas Pfizer/BioNTech BNT162b2 e Moderna mRNA-1273 COVID-19 [4]. Isso também foi inédito no processo de aprovação, sendo o mais rápido para qualquer vacina [5], deixando muitas preocupações em relação à segurança a longo prazo [6], que era difícil de avaliar devido ao desmascaramento dos ensaios clínicos iniciais [7].
Embora a tecnologia de entrega de LNPs tenha sido usada anteriormente para entregar moléculas pequenas, ela só recentemente foi usada para entregar RNA. Os LNPs são vantajosos para atingir o tecido cerebral, pois podem atravessar a barreira hematoencefálica (BHE) [8,9]. A primeira droga usada e LNP para entregar RNA foi uma pequena droga baseada em RNA de interferência (siRNA), conhecida como Onpattro (Alnylam Pharmaceuticals), aprovada pela primeira vez em 2018 para o tratamento de polineuropatias [10].
Dada a novidade da tecnologia e a escassez de dados nos quais a aprovação se baseou (que também estava sujeita a questões de integridade de dados [11]), os efeitos de longo prazo não podem ser definitivamente descartados, especialmente porque muitas das alegações fundamentais nas quais a aprovação se baseou foram contestadas por experimentos recentes [12,13,14]. Por exemplo, em contraste com as alegações de que a injeção permaneceu no local da injeção [15], e que a proteína spike só seria expressa por um curto período de tempo (com base na labilidade do RNA não pseudouridilado [16]), o conteúdo e os produtos das vacinas COVID-19 foram encontrados na corrente sanguínea da maioria dos vacinados estudados dentro de horas a dias [12].
A primeira alegação foi baseada na administração intramuscular [15], e a segunda alegação foi baseada na labilidade do RNA [17], com uma meia-vida típica de RNA de minutos [18]; no entanto, estudos de biodistribuição encontraram expressão significativa de picos em outros tecidos e órgãos [12], e os pesquisadores encontraram tanto o mRNA da vacina quanto a proteína spike (que é codificada pela sequência vacinal) dois meses após a administração [14], e até quatro meses após a vacinação [13]. Um estudo de pré-impressão de pessoas com SARS-CoV-2 negativo pós-vacinação Sintomas longos COVID-19-like mostraram persistência da proteína spike, em média, 105 dias após a vacinação [19]. Pacientes longos de COVID-19 (pós-infecção por SARS-CoV-2) mostram persistência da proteína spike até 15 meses [20]. Outro estudo mostrou persistência da proteína spike no intestino de pacientes com COVID-19 longo, mas não na corrente sanguínea.
As proteínas spike podem ser acondicionadas em exossomos [13], podendo resultar em inflamação e ativação imune [21,22] em órgãos e tecidos distantes do local da injeção [13]. As vesículas extracelulares são capazes de atravessar a barreira hematoencefálica [23], e os LNPs, assim como os exossomos, trocarão mais facilmente em vasos de pequeno diâmetro com baixas taxas de fluxo (isto é, capilares e pequenos vasos) [24]. É importante ressaltar que a proteína spike parece impactar adicionalmente a permeabilidade da barreira hematoencefálica [25,26]. Esses resultados desafiam o fundamento mecanicista inicial sobre o qual se assenta a presunção de segurança.
Em comparação com outras vacinas, as vacinas COVID-19 têm uma taxa de eventos adversos muito maior [27]. Achados histopatológicos e autópsias daqueles que morreram após a vacinação reforçam o papel causal da vacina em mortes [28], mais comumente por eventos vasculares. Programas de farmacovigilância em vários países observaram um sinal de segurança para miocardite na população vacinada COVID-19 [29,30,31]. Uma pesquisa norte-americana constatou que 19% dos casos de miocardite não haviam se recuperado aos 90 dias após o início [32]. Além disso, a triagem de receptores da vacina BNT162b2 entre meninos de 13 a 18 anos em um estudo tailandês revelou que 2,3% dos meninos tinham pelo menos um biomarcador cardíaco elevado ou avaliação laboratorial positiva, e 29% tinham pelo menos uma manifestação cardíaca, como taquicardia, palpitação ou miopericardite [33]. Dada esta informação, e dado o uso ubíquo das vacinas COVID-19, é possível que o dano subclínico generalizado exista na população vacinada COVID-19. Estruturalmente, a proteína spike, particularmente o domínio de ligação ao receptor (RBD) da subunidade S1, tem atraído muita atenção, pois é o aspecto mais proeminente das glicoproteínas do capsídeo viral [34] (Consiste em spike (S) e nucleocapsídeo (N)) glicoproteínas. A entrada celular é mediada pela ligação do Spike RBD à Enzima Conversora de Angiotensina II (ECA2) [35]. Portanto, impedindo essa ligação através da inibição alostérica, é possível impedir a entrada de virions SARS-CoV-2 na célula e a infecção subsequente [36].
Uma estratégia para inibir a ligação de S1 RBD a ACE2 tem sido empregada no desenvolvimento de vacinas SARS-CoV-2 [37]. As vacinas de mRNA codificam exclusivamente proteínas spike, e o direcionamento mono-antigênico pode criar oportunidades de escape imunológico por variantes [38], uma vez que as vacinas de mRNA não interrompem a transmissão [39]. Observa-se pressão de seleção positiva sobre resíduos da proteína spike devido à vacinação generalizada, embora estes não possam ser definitivamente relacionados causalmente [40,41].
Este artigo se propõe a descrever primeiramente os mecanismos da patologia relacionada à proteína spike e os fatores que os afetam (por exemplo, características do paciente) e seus biomarcadores e diagnósticos relevantes. O objetivo, então, é introduzir terapêuticas promissoras, baseadas em evidências mecanicistas ou clínicas, e resumir a base de evidências de cada intervenção, para que profissionais e cientistas possam ser orientados quanto ao desenvolvimento terapêutico. Outros artigos cobrem a fisiopatologia de COVID-19 longo, bem como fornecem uma lista de terapêuticas sob investigação [42], e uma revisão recente descreve as semelhanças entre COVID-19 longo e COVID-19 lesão vacinal [43]. Esta revisão é única na medida em que fornece uma discussão integrada do mecanismo da doença para a síndrome da vacinação pós-COVID-19 e COVID-19 longa, que são difíceis de distinguir em muitos casos, e resume as modalidades de tratamento disponíveis para aqueles que experimentam sintomas.
2. Métodos
Esta revisão começa resumindo os mecanismos do dano da proteína spike, seja da doença COVID-19 ou da vacinação COVID-19. Abordamos também os aspectos clínicos, que podem afetar o curso da doença. A revisão então passa para mecanismos terapêuticos, que podem abordar a proteína spike por diferentes caminhos.
Para intervenções terapêuticas para essas condições (COVID-19 longo e lesão vacinal) com um mecanismo plausível de ação contra a proteína spike, estas são mostradas na seção de resultados. Ensaios clínicos relevantes são adicionados, e qualquer evidência direta ou evidência proxy de eficácia (como eficácia contra a doença COVID-19 original) é incluída na coluna mais à direita.
Além disso, incluímos ensaios clínicos sobre COVID-19 longo e lesão vacinal na Tabela S1. Uma busca por ensaios clínicos para a condição “COVID longo OU COVID-19 longo” em ClinicalTrials.gov revelou 317 estudos. Uma busca por ensaios clínicos sobre eventos adversos vacinais revelou que um estudo usou rutina e suco de amora rico em glicosídeos para reduzir eventos adversos à injeção de C19 [44]. Outros estudos, embora não tratem especificamente a resposta imune, administram terapia juntamente com a vacinação para observar mudanças na resposta. Estes incluem espermidina [45], probióticos [46], um suplemento à base de levedura rico em selênio e zinco [47], ésteres de estanol vegetal [48], cogumelos [49], exercícios de músculo deltoide (para dor local) [50], tratamento manipulativo osteopático [51,52], metformina [53], ferro [54], ergoferon [55], dieta cetogênica [56] e imunossupressores [57,58].
É difícil avaliar a base probatória de cada tipo de intervenção, pois poucas meta-análises foram realizadas. Por exemplo, uma pesquisa na Biblioteca de Colaboração Cochrane para “COVID-19 pós-agudo” produz uma revisão relevante sobre a correção da disfunção olfatória, encontrando evidências limitadas para a utilidade das terapias propostas [59]. Além disso, 46 estudos relevantes concluídos para o termo de pesquisa “COVID longo” existem em ClinicalTrials.gov (8 de janeiro de 2023). Como existem poucas revisões sistemáticas, pretendemos resumir a base probatória das intervenções conhecidas actualmente nos ensaios clínicos para o tratamento da lesão COVID-19 longa e COVID-19 vacinal são mostradas na tabela S1. Há uma única revisão sobre o tratamento da lesão da vacina COVID-19 que poderia ser encontrada, que está incluída na Tabela S1.
3. Fisiopatologia
3.1. Mecanismos de Dano
Como mencionado anteriormente, embora fosse esperado que os mRNAs sintéticos encapsulados em LNP permanecessem no local da injeção e se degradassem rapidamente, há evidências substanciais de que eles entram na corrente sanguínea [60], depositam-se em outros tecidos [61] e até mesmo no leite materno de lactantes [62]. A subunidade S1 da proteína spike pode lesar o revestimento endotelial dos vasos sanguíneos [63,64,65]. Partículas vacinais na corrente sanguínea podem causar uma resposta inflamatória significativa nos vasos sanguíneos [66].
Existem várias hipóteses para os mecanismos de COVID-19 longo, incluindo a desregulação imune, a autoimunidade, a disfunção endotelial, a activação da coagulação, e a persistência viral latente [67,68], embora esta revisão se concentre nos elementos comuns à infecção COVID-19 e à lesão vacinal. As complicações cardiovasculares, particularmente a formação de microtrombos, caracterizam-se tanto nas etiologias de COVID-19 longo [69,70] como na lesão vacinal de COVID-19 [71].
A proteína spike do SARS-CoV-2 (infecção ou vacina produzida) pode ligar-se ao receptor ACE2 nas plaquetas, levando à sua ativação [72], e pode causar coágulos sanguíneos resistentes ao fibrinogênio [73]. Fragmentos de proteína spike também podem ser amiloidogênicos por conta própria [74]. Vários relatórios demonstram níveis elevados de troponina em sintomas cardíacos após a vacina COVID-19 [75].
Ontologicamente, tanto a infecção quanto a vacinação expressam a proteína spike, embora existam algumas diferenças sutis entre a proteína spike gerada pela vacina e a proteína spike gerada pela infecção. É importante ressaltar que a proteína spike codificada pelas vacinas é estática e não sofre evolução, enquanto a proteína spike produzida pela infecção evolui à medida que o vírus evolui [76,77]. Há uma exceção a isso, que é quando a vacina é atualizada, como é nos reforços bivalentes da Pfizer e da Moderna, que expressam a proteína spike tanto da sublinhagem B.1.1.529 (ômicron) BA.5 quanto da cepa ancestral WA1/2020 [78]. A outra distinção importante entre a espícula vacinal e a espícula da infecção é o estado estabilizado da pré-fusão na espícula vacinal, que resulta em uma afinidade de ligação ACE2 aumentada em comparação com as proteínas spike geradas pela infecção por SARS-CoV-2 [79]. A diferença na proteína spike do SARS-CoV-2 circulante (na população) para a proteína spike (vacina ou infecção gerada) do imprinting imune inicial tem implicações importantes para o escape imune [77,80] e danos imunomediados [81]. O escape imunológico é demonstrado em estudos populacionais que demonstram diminuição da eficácia vacinal [82].
Em 2021, uma investigação abrangente revelou alterações fisiopatológicas consistentes após a vacinação com vacinas COVID-19, incluindo alterações da expressão gênica de células imunes [83].
3.2. Observações Clínicas
Embora não exista uma definição oficial para ‘Síndrome pós-COVID-19-Vaccine’, uma correlação temporal entre receber uma vacina COVID-19 e o início ou agravamento das manifestações clínicas de um paciente é suficiente para fazer o diagnóstico de uma lesão induzida pela vacina COVID-19 quando os sintomas são inexplicáveis por outras causas simultâneas. Deve-se, no entanto, reconhecer que há uma sobreposição significativa entre os sintomas e as características da síndrome COVID-19 longa [84] e da síndrome pós-COVID-19-Vaccine [85]. No entanto, um número de características clínicas parecem ser distintivas da síndrome vacinal pós-COVID-19; Mais notavelmente, sintomas neurológicos graves (particularmente neuropatia de fibras pequenas) parecem ser mais comuns após a vacinação [86,87,88]. Para complicar ainda mais, os pacientes com COVID-19 longo são frequentemente vacinados [89], tornando a questão da definição mais difícil.
Infelizmente, apenas o exame post mortem até o momento pode provar relação causal quando os tecidos danificados demonstram a presença de proteína spike e ausência de proteína nucleocapsídea (somente SARS-CoV-2) [90].
A verdadeira magnitude da síndrome pós-COVID-19-Vaccine é desconhecida, como os dados são limitados a ensaios clínicos de curta duração. A partir de uma pesquisa com indivíduos vacinados, aproximadamente 1% necessitou de atenção médica imediatamente após a vacinação [91]. Um estudo de coorte nacional de veteranos dos EUA relatou reações adversas em 8,5% dos receptores da vacina da Pfizer e 7,9% daqueles que receberam a vacina da Moderna [92].
Vários fatores estão associados a um risco aumentado de eventos adversos; Estes incluem:
-
Genética: parentes de primeiro grau de pessoas que sofreram uma lesão vacinal parecem estar em um risco muito alto de lesão vacinal. Pessoas com mutação no gene da metilenotetrahidrofolato redutase (MTHFR) [93] e aquelas com síndromes do tipo Ehlers-Danlos podem ter um risco aumentado de lesão. Níveis aumentados de homocisteína foram associados a piores resultados em pacientes com COVID-19 [94,95]. Níveis elevados de homocisteína podem potencializar a lesão microvascular e as complicações trombóticas associadas à lesão vacinal relacionada à proteína spike [96,97].
-
Carga de mRNA e quantidade de proteína spike produzida: isso pode estar ligado a lotes específicos de vacinas que contêm uma maior concentração de mRNA devido a variações na qualidade de fabricação, bem como heterogeneidade dentro do frasco [98].
-
Tipo e lote da vacina: foram observadas variações nos níveis de reações adversas, dependendo do fabricante da vacina [91].
-
Número de vacinas administradas: o risco de aumento de anticorpos (EAM) aumenta a cada exposição ao vírus ou a uma vacina. Observou-se também correlação negativa inversa das doses administradas, bem como da efetividade [99].
-
Sexo: a maioria das pessoas vacinadas é do sexo feminino [100], e as vacinas historicamente têm efeitos específicos do sexo [101].
4. Intervenções Terapêuticas
Existem vários meios não específicos de neutralizar os efeitos da lesão vacinal COVID-19 longa e pós-COVID-19. Estes incluem suporte nutricional para a regulação imunológica geral e para a saúde geral [104], bem como terapêuticas mais específicas, específicas da proteína spike.
As metades terapêuticas não específicas incluem a otimização nutricional, como patologias diet-relacionadas, incluindo a obesidade [105] e a diabetes tipo 2 [106], foram associadas com resultados piores da infecção COVID-19. Além disso, a glicemia elevada facilita várias etapas do ciclo de vida viral e progressão da infecção [107], motivando a redução da ingestão de açúcar e carboidratos refinados, que estão associados ao aumento do açúcar no sangue. Além disso, a adoção de uma dieta integral à base de plantas está associada à diminuição do estresse oxidativo e da inflamação [108] e melhores condições cardiovasculares. Esses impactos positivos são atribuídos ao seu perfil nutricional, composto por antioxidantes, vitaminas, minerais e compostos fenólicos contendo fitoquímicos, que podem exercer efeitos antioxidantes, anti-inflamatórios e outros efeitos benéficos [109,110].
A microbiota desempenha um papel fundamental na indução, treinamento e função do sistema imunológico do hospedeiro e, assim, molda as respostas aos seus desafios [111]. A composição do microbioma intestinal foi significativamente alterada em pacientes com COVID-19 em comparação com indivíduos não-COVID-19, independentemente de os pacientes terem recebido a medicação [112]. Os pesquisadores disseram que os pacientes com doença grave exibem altos níveis plasmáticos no sangue de citocinas inflamatórias e marcadores inflamatórios. Além disso, dada a composição alterada da microbiota intestinal em indivíduos infectados por SARS-CoV-2, há envolvimento substancial do trato gastrointestinal durante a infecção. Estes resultados sugerem que a composição da microbiota intestinal está associada com a magnitude da resposta imune à COVID-19 e o dano tecidual subsequente e, portanto, poderia desempenhar um papel na regulação da gravidade da doença. Os cientistas igualmente encontraram que, porque um pequeno subconjunto de pacientes mostraram disbiose da microbiota intestinal, ou desequilíbrio, mesmo 30 dias após a recuperação, esta poderia ser uma explicação potencial para por que alguns sintomas persistem em COVID-19 longo [113].
Dada a influência intrincada da microbiota intestinal (GM) nos efetores imunes do hospedeiro e no perfil inflamatório subsequente, a composição e a função do GM podem contribuir para explicar a resiliência/fragilidade individual em relação à COVID-19 e/ou a resposta à terapêutica (vacinas), que merecem mais pesquisas [114]. A diversidade microbiana pode ser melhorada com o consumo de muitos prebióticos e probióticos, como chucrute e kimchi.
O projeto e a descoberta dos inibidores da proteína spike seguiram um processo típico de reaproveitamento de drogas. Dada a semelhança estrutural da proteína spike do SARS-CoV-2 com outros coronaviruses [115.116], os compostos que trabalham para estes poderiam ser potencialmente reaproveitados para a inibição da espícula do SARS-CoV-2.
Tipicamente, uma vez identificado um composto prospectivo para reaproveitamento, ele é testado usando um ensaio de ligação ao ligante (LBA) [117]. Estes ensaios podem fornecer informações sobre afinidade e cinética de ligação, bem como estequiometrias de ligação e até mesmo efeitos cooperativos [117].
O próximo nível de verificação pode ser um ensaio in vitro para inibição viral em cultura celular, onde as células estão infectadas com um vírus, e os níveis virais ou título (concentração) são medidos pela contagem de placas virais [118] ou medição dos níveis de ácido nucleico viral (NA) [119]. As células de controle são comparadas com as células tratadas. Embora a abordagem tenha limitações, ao não considerar a dinâmica de corpo inteiro de um vírus [120], ela pode servir como um ponto de partida útil.
Estudos in vivo são um nível adicional de verificação, que mostram o impacto da intervenção em um modelo animal. Além dos estudos in vivo, existem os estudos clínicos, que são tipicamente de dois tipos de desenho: estudos observacionais e ensaios clínicos randomizados (ECRCs) [121].
Até o momento, pouca ou nenhuma orientação foi fornecida pelas autoridades de saúde sobre como gerenciar a doença relacionada à proteína spike, deixando a cargo de cientistas e médicos independentes desenvolverem. Em relação à Síndrome de Trombocitopenia Trombótica (TTS) induzida pela vacina COVID-19, uma revisão de 2021 fez sugestões sobre o manejo, incluindo imunoglobulina intravenosa, anticoagulantes e plasmaférese em casos graves [122]. Esses compostos são suplementos nutricionais e produtos naturais, com alguns fármacos reaproveitados (Tabela 1 e Tabela 2).
Essa lista aponta para as evidências disponíveis sobre cada terapia e as avança para uma investigação mais aprofundada. A terapêutica a seguir funciona através de diferentes mecanismos, mas nos concentramos principalmente nas proteínas que se ligam diretamente à proteína spike para melhorar a eliminação. Aqui, resumimos estudos com diferentes níveis de evidência para suas respectivas eficácias, desde predições in silico, que podem ser baseadas em predições de ligação ou associações biológicas de sistemas, até aqueles que mostram atividade em um ensaio in vitro ou livre de células, estudos in vivo e qualquer evidência clínica ou epidemiológica.
Dadas as muitas incertezas em torno da duração da produção da proteína spike e das variáveis que determinam a produção, a adoção de uma abordagem preventiva parece sensata, desde que as intervenções propostas sejam seguras. Ainda não se sabe se a recuperação completa da lesão da vacina COVID-19 é possível. No entanto, sugerimos direcionar vários processos diferentes para reduzir os sintomas associados à lesão vacinal e COVID-19 longo. Estes incluem:
- (1)
-
Estabelecendo um microbioma saudável
- (2)
-
Inibição da clivagem e ligação da proteína spike (interrompendo os danos contínuos)
- (3)
-
Limpar a proteína spike do corpo (limpar os agentes prejudiciais)
- (4)
-
Curar os danos causados pela proteína spike (restaurando a homeostase e impulsionando o sistema imunológico)
Essas categorias não são claramente separadas, pois os compostos que se ligam à espícula podem tanto inativá-la impedindo sua ligação à ACE2, quanto auxiliar na sua eliminação. Existem muitas vias biológicas através das quais um determinado efeito pode ocorrer. Para inibir os efeitos deletérios da proteína spike, é possível atingir a clivagem da furina, seja ligando-se diretamente ao próprio sítio de clivagem da furina [123,124,125] ou interferindo na reação de serinoprotease [126,127,128] para bloquear a interação ligando-se à ACE2 [129], diminuindo a expressão da ACE2 [130], inibindo a transição para a conformação ativa da proteína S [131], ou ligando o RBD da proteína spike e inibindo alostericamente a interação com a ACE2 [132] (Figura 1). A limpeza das proteínas spike também pode ser realizada pelo aumento da autofagia, que limpa as proteínas e recicla seus aminoácidos [133].
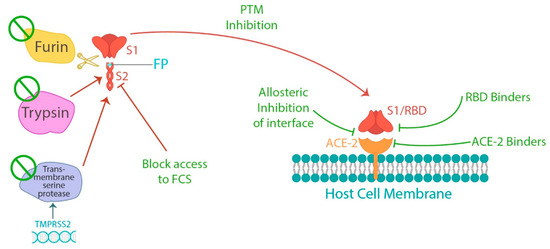
Gráfico 1. O processo de clivagem da proteína spike em subunidades S1 e S2 e subsequente ligação do domínio de ligação do receptor S1 (RBD) ao receptor da enzima conversora de angiotensão2 (ACE2) nas células hospedeiras. Cada um dos diferentes subprocessos apresenta oportunidades de interferência na ligação da espícula à ACE2, bem como um meio potencial de tratar patologia relacionada à proteína spike.
4.1. Estabelecimento de um microbioma saudável
O estado do microbiome é um critério essencial para a progressão da infecção aguda de COVID-19, COVID-19 longo e síndrome pós-vacina [134,135,136,137,138]. Pacientes com síndrome pós-vacinal classicamente apresentam disbiose grave com perda de Bifidobacterium [139,140,141]. Uma dieta integral, baseada em plantas pode melhorar os resultados em COVID-19 [142,143,144], e as pessoas que seguem dietas à base de plantas, em média, experimentaram sintomas COVID-19 menos graves [145]. Fontes dietéticas de probióticos incluem laticínios fermentados [146], sementes de chia [147], glucomanano [148,149], e suplementos [150].
A diversidade e riqueza do microbioma podem ser melhoradas através de uma dieta rica em fibras prebióticas e probióticos, particularmente alimentos fermentados, que podem subsequentemente reduzir a inflamação [151].
4.2. Prevenir os danos causados pela proteína spike
Inibindo a clivagem da proteína spike
O local de clivagem da furina no SARS-CoV-2 foi sugerido como uma razão para sua infectividade aumentada em relação ao SARS-CoV [152], que teve uma taxa de letalidade mais alta, que foi muito menos infecciosa [153]. A clivagem da proteína spike de comprimento total em subunidades S1 e S2 é essencial para a entrada do SARS-CoV-2 nas pilhas do pulmão humano [126,154,155,156]. A espícula completa está presente tanto na infecção por SARS-CoV-2, quanto na vacinação, e é a única proteína comum à infecção por SARS-CoV-2 e à vacinação (é a única proteína presente na vacinação) [157].
A espícula produzida pela vacina tem uma diferença importante em comparação com a espícula do SARS-CoV-2 – a inclusão de duas mutações da prolina para estabilizar o estado de pré-fusão da proteína spike. Estes estão relacionados com BNT162b2 [158] da Pfizer, mRNA-1273 [159] da Moderna, Ad26.COV2.S [160] de Johnson e NVAX-CoV2373 [161] da NovaVax. Isso foi descoberto pela primeira vez no contexto da MERS [162]. Outras vacinas aparentemente codificam a proteína spike de tipo selvagem, incluindo a ChAdOx1 [163] da AstraZeneca e a CoronaVac da SinoVac [164].
Essas mutações duplas de prolina apresentadas nas vacinas de mRNA estabilizam o estado de pré-fusão, embora alguma clivagem ainda ocorra [162,165,166], e, curiosamente, as mutações produzem um produto de clivagem desconhecido de 40 kDa, onde os produtos típicos de clivagem para a proteína spike selvagem são de 80 kDa [166]. Como tal, o alvo da clivagem da proteína spike provavelmente fará a diferença na COVID longa, bem como a lesão vacinal das vacinas que codificam a proteína spike do tipo selvagem de comprimento total (AstraZeneca, SinoVac e outras), embora isso possa ter menos impacto nas vacinas que codificam a proteína spike pré-estabilizada pela fusão (Pfizer, Moderna, Johnson e Johnson, NovaVax e outras).
Notavelmente, a clivagem do alvo também foi identificada como uma modalidade terapêutica no contexto da COVID-19 aguda [167.168], que pode ocorrer através de pelo menos três vias distintas: clivagem por furina, tripsina ou serina protease transmembrana [167,168,169].
4.3. Inibindo a ligação à proteína spike
Um dos mecanismos terapêuticos mais diretos é buscar compostos que interrompam a interface ACE2/Spike, seja através da ligação ACE2 ou spike no isolamento, ou interrompendo a própria interface. Este problema é um problema estérico e conformacional, para o qual a predição computacional usando modelos estruturais é altamente aceitável. Muitos estudos computacionais da proteína spike e dos compostos ligantes da ACE2 foram realizados, e alguns desses acertos foram desenvolvidos através de LBAs, estudos in vitro, estudos in vivo em modelos animais e, por último, ensaios clínicos com seres humanos. Poucos dos compostos atingem o estágio final, embora vários com este mecanismo de ação tenham sido investigados. As mais promissoras foram a ivermectina e a quercetina, já que a previsão computacional mostrou que elas se ligam à espícula. Se a espícula está ligada no domínio de ligação ao receptor (RBD), a interação com os receptores ACE2, pelo qual a proteína spike exerce seu efeito inflamatório, também é inibida.
Da mesma forma, compostos que se ligam ao receptor ACE2 também podem competir antagonisticamente com a proteína spike por um número limitado de locais receptores. Por exemplo, o medicamento para diabetes metformina foi identificado como um potencial agente terapêutico COVID-19 longo devido a este mecanismo de ação. Diminuir o nível de ligação ativa da espícula à ACE2 tem implicações terapêuticas.
4.4. Limpando a proteína spike
Até agora, discutimos maneiras de inibir os impactos da proteína spike no sistema do hospedeiro. É importante ressaltar que, para progredir além disso, é necessário eliminar a proteína spike. Isto pode ser conseguido através da upregulation das vias degradativas da proteína no corpo através da upregulation da autofagia. A autofagia pode ser regulada pelo jejum [170] e pela restrição calórica [171], especialmente se a proteína estiver reduzida [172]. A autofagia, em muitos casos, não exige a cessação completa da ingestão alimentar (os protocolos estão disponíveis em https://COVID19criticalcare.com/treatment-protocols/, acessado em 15 de abril de 2023). A diminuição acentuada da ingestão proteica pode regular as vias de autofagia [173], e isso pode ser realizado ainda durante a alimentação, o que torna isso mais acessível como protocolo. O jejum regular também foi associado com melhores resultados de COVID-19 agudo [174].
A espermidina, um composto polianiônico encontrado em altas concentrações no germe de trigo [175], pode estimular poderosamente a autofagia [176]. Outros fatores que influenciam a autofagia são a exposição aguda ao calor, como se experimentaria em uma sauna [177,178], o consumo de flavonoides [179], compostos fenólicos [180,181] e café [182]. O resveratrol também pode induzir jejum, pois atua como um mimético de restrição proteica [183], e a metformina, um medicamento para diabetes, pode influenciar a sinalização da autofagia [184]. Surpreendentemente, a exposição ao frio, além da exposição ao calor, também aumenta a autofagia [185,186]. O oxigênio hiperbárico [187] e a ozonioterapia [188] também podem estimular a autofagia.
4.5. Curar os danos
Depois que o processo de dano foi atenuado, é necessário curar o dano que ocorreu. A fase de cicatrização requer a normalização da resposta imune, a redução da inflamação persistente (como o alvo da interleucina 6 [189]) e a abordagem de qualquer dano agudo nos tecidos afetados, particularmente o dano cardiovascular [69,70,71]. A redução de danos também pode significar a redução do nível de coagulação do sangue se a coagulação estiver presente e a reparação de qualquer dano ao órgão, se relevante. O estágio de cicatrização requer a normalização da resposta imune, a redução da inflamação persistente (como o direcionamento da interleucina 6 [189]) e a abordagem de qualquer dano agudo em quaisquer tecidos afetados, o que, para nossos propósitos, inclui o sangue. Micro-coágulos são um possível fator etiológico em COVID-19 longo [190,191,192], bem como lesão vacinal COVID-19 [193]. A redução de danos também pode significar a redução do nível de coagulação do sangue, se houver coagulação, e a reparação de qualquer dano ao órgão, se relevante. Os sofredores de COVID-19 longo foram encontrados para ter uma resposta inflamatório mais alta à infecção COVID-19 inicial do que aqueles que se recuperam completamente de COVID-19 [194], assim que os medicamentos anti-inflamatórios e imunomoduladores foram identificados como terapêuticas COVID-19 longas potenciais.
Medicamentos anticoagulantes, como a aspirina, podem ser úteis para aliviar as complicações cardiovasculares da COVID-19 [195,196], pois têm uma longa história de uso na melhoria do fluxo sanguíneo e na redução de coagulopatias [197,198,199].
Outro composto útil para quebrar coágulos sanguíneos é a nattokinase, que é um fibrinolítico encontrado em soja fermentada (espécie bacteriana Bacillus subtilis var. natto) [200,201]. Experimentos têm demonstrado que ela degrada potentemente a proteína spike [202,203], o que é um benefício adicional, além de suas propriedades fibrinolíticas e anticoagulantes [204].
4.6. Terapêutica potencial
Na Tabela 1, agrupamos as terapêuticas por mecanismo e estágio (conforme nossas definições acima) e incluímos informações sobre suas origens. Nossa categorização por fontes é baseada na classificação de produtos naturais (NP) ou fármacos (PD). Para os produtos naturais, incluímos o(s) organismo(s) fonte(s) mais comum(is) com base em seu nome científico para consistência.
Os compostos farmacêuticos com aplicabilidade plausível para o tratamento da COVID-19 longa e síndrome pós-vacinal estão listados na Tabela 1.
Tabela 1. Compostos farmacêuticos com mecanismos plausíveis de ação contra patologias relacionadas à proteína spike.
Da mesma forma, compostos naturais e suplementos com aplicabilidade plausível para o tratamento da COVID-19 longa e síndrome pós-vacina estão listados na Tabela 2.
Tabela 2. Compostos naturais e suplementos com mecanismos plausíveis de ação contra patologias relacionadas à proteína spike.

5. Discussão
A melhora dos sintomas e a recuperação de um grande número de pessoas em todo o mundo da COVID longa e da síndrome e lesão pós-vacina requer o uso de terapias integrativas não invasivas que podem ser dimensionadas e administradas de forma descentralizada. É importante disseminar esse conhecimento para o público leigo para que ele possa mitigar seus riscos individuais e os de seus entes queridos. Embora seja difícil enumerar a verdadeira escala de distúrbios de coagulação pós-vacinação ou pós-COVID, houve um aumento apreciável em incidentes cardíacos [29], derrames (hemorragias intercerebrais [338]) e excesso de mortalidade não-COVID [339.340]. Um aumento significativo na mortalidade total devido a uma vacina não é inédito, uma vez que a vacina DTP administrada na Guiné-Bissau na década de 1980 aumentou a mortalidade infantil em quatro vezes em comparação com a mortalidade não vacinada [341].
Embora a magnitude do impacto da síndrome ou lesão da vacina COVID-19 longa e pós-COVID-19 não seja clara, é importante se preparar para as consequências potenciais tendo informações prontas para disseminação, bem como realizar pesquisas sobre terapêuticas promissoras para aliviar os danos causados pela proteína spike e outros mecanismos potenciais de dano, como a integração do DNA [342]. Uma limitação deste estudo é que ele se concentra na patologia relacionada à proteína spike e pode deixar de fora outras possibilidades, como alergias a componentes da vacina ou outras etiologias de doenças. A síndrome vacinal longa COVID-19 e pós-COVID-19 são doenças multifacetadas, com manifestações altamente variadas; Como tal, o desenvolvimento de diagnósticos objetivos é importante no tratamento dos pacientes. As terapias discutidas nesta revisão têm uma base probatória variável e podem servir como pontos de partida para o desenvolvimento de terapias para aliviar patologias relacionadas à proteína spike nos próximos anos.
Pesquisas futuras requerem validação dos tratamentos descritos nesta revisão por ensaios clínicos randomizados (ECR), estudos observacionais e estudos laboratoriais de mecanismo biológico. Além disso, a integração da pesquisa atual sobre distúrbios relacionados à proteína spike é útil. Uma possibilidade é a aplicação de ferramentas de biologia de sistemas para descrever as perturbações em diferentes vias biológicas influenciadas pela proteína spike. Quando esse modelo existe, é possível tratar as manifestações agudas da doença enquanto ainda limpa a proteína spike do corpo.
Os governos e os serviços nacionais de saúde começam a aceitar a magnitude da tarefa que têm pela frente. Esta revisão delineia algumas das terapias mais promissoras de uma perspectiva mecanicista e probatória biológica. Esperamos que este artigo seja utilizado na construção de protocolos de tratamento para tratar essas condições altamente relacionadas em suas diversas manifestações da doença, priorizando não apenas a segurança e eficácia, mas o custo e a disponibilidade para um grande número de pessoas.
Materiais Complementares
As seguintes informações de suporte podem ser baixadas em: https://www.mdpi.com/article/10.3390/microorganisms11051308/s1, Tabela S1: Visão geral dos ensaios clínicos para lesões de vacinas COVID-COVID longa e COVID-19.
Contribuição dos autores
Conceituação, M.T.J.H.; metodologia, M.T.J.H.; investigação, M.T.J.H., C.P., P.M. e T.A.L.; redação – elaboração de minuta original, M.T.J.H.; redação – revisão e edição, M.T.J.H., C.P., P.M. e T.A.L.; supervisão e administração de projetos, M.T.J.H.; aquisição de financiamento, T.A.L. Todos os autores leram e concordaram com a versão publicada do manuscrito.
Financiamento
Este artigo foi financiado por doações públicas para a iniciativa do Conselho Mundial de Saúde.
Declaração de disponibilidade de dados
Conjuntos de dados disponíveis publicamente foram analisados neste estudo. Os dados sobre os ensaios clínicos podem ser consultados em clinicaltrials.gov.
Confirmações
Os autores agradecem as contribuições de Francesca Havens, Dana F. Flavin e A.J. Além disso, os autores agradecem as contribuições seminais da FLCCC Alliance e a publicação de protocolos para o manejo da vacina (https://COVIDCOVID19criticalcare.com/treatment-protocols/i-prevent-vaccine-injury/, acessado em 15 de abril de 2023).
Conflitos de Interesse
M.T.J.H., C.P. e T.A.L. fazem parte do Comitê de Saúde e Ciência do Conselho Mundial de Saúde, uma iniciativa centrada nas pessoas da empresa sem fins lucrativos Community Interest Company (CIC) EbMCsquared, para promover a saúde holística.
Referências
- Ribeiro, A.; Oliveira, E.; Oliveira, L.; Apelação, C.; Oliveira, C.; Oliveira, E.; Oliveira, J.; Oliveira, A.; Oliveira, D.; Roser, M. Pandemia do coronavírus (COVID-19). Nosso Mundo em Dados 2020. Disponível online: https://ourworldindata.org/coronavirus (acesso em 1º de outubro de 2022).
- Equipe, G. Produção de vacinas COVID-19 até 31 de janeiro de 2022. Disponível online: https://globalcommissionforpostpandemicpolicy.org/covid-19-vaccine-production-to-january-31st-2022/ (acesso em 1º de outubro de 2022).
- Oliveira, M.T.J.; Oliveira, J.; Lourenço, T.; A novidade das vacinas virais de mRNA e danos potenciais: uma revisão de escopo. J 2023, 6, 220-235. [Google Acadêmico] [Referência Cruzada]
- ARQUIVO: Condições de autorização para a vacina COVID-19 Pfizer/BioNTech (Regulamento 174). Disponível online: https://www.gov.uk/government/publications/regulatory-approval-of-pfizer-biontech-vaccine-for-covid-19/conditions-of-authorisation-for-pfizerbiontech-covid-19-vaccine (acesso em 1º de outubro de 2022).
- Bola, P. A busca relâmpago por vacinas COVID – e o que isso significa para outras doenças. Natureza 2020, 589, 16–18. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, P.; Stahel, V.P. Revisar a segurança das vacinas COVID-19 MRNA: uma revisão. Paciente Saf. 2021, 15, 20. [Google Acadêmico] [CrossRef] [PubMed]
- Doshi, P. Vacinas COVID-19: Na corrida pela aprovação regulatória, precisamos de mais dados? BMJ 2021, 373, n1244. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, M.L.; Oliveira, R.; Craparo, E.F. Capítulo Doze – Nanopartículas lipídicas para o direcionamento de drogas para o cérebro. em Métodos em Enzimologia; Düzgüneş, N., Ed.; Imprensa Acadêmica: Cambridge, MA, EUA, 2012; Volume 508, pp. 229-251. [Google Acadêmico]
- Ribeiro, F.H.; Oliveira, A.; Pereira, M.N.; Oliveira, A.A.; Harshita; Oliveira, M.S.; Oliveira, J.M.; Oliveira, O.; Oliveira, M.A.; Oliveira, E.G.; Nanoformulações Lipídicas no Tratamento de Distúrbios Neurológicos. Medicamento. Metab. Apocalipse 2020, 52, 185–204. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, A.; Oliveira, M.A.; Oliveira, M.; Pereira, J.; Oliveira, M.; Barros, A.; Oliveira, A.; Oliveira, X.; Oliveira, J.M.; Oliveira, D.D.; et al. A História de Onpattro e a Tradução Clínica de Nanomedicamentos Contendo Drogas à Base de Ácido Nucleico. Nanotechnol. 2019, 14, 1084–1087. [Google Acadêmico] [CrossRef] [PubMed]
- Covid-19: Pesquisador denuncia problemas de integridade de dados no teste da vacina da Pfizer. BMJ 2021, 375, n2635. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.F.; Oliveira, C.-A.; Oliveira, M.; Oliveira, A.; Pereira, A.C.; Oliveira, M.; Oliveira, A.; Oliveira, A.; Oliveira, X.; Pereira, R.R.; Antígeno da vacina contra o coronavírus 2 da síndrome respiratória aguda grave circulante (SARS-CoV-2) detectado no plasma de receptores da vacina MRNA-1273. Clin. Infetar. Dis. 2022, 74, 715-718. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Perincheri, A.; Ribeiro, A.; Oliveira, C.; Ribeiro, A.; Oliveira, R.M.; Mohanakumar, T. Cutting Edge: Exossomos circulantes com proteína spike COVID são induzidos pela vacinação BNT162b2 (Pfizer-BioNTech) antes do desenvolvimento de anticorpos: um novo mecanismo para a ativação imune por vacinas MRNA. J. Imunol. 2021, 207, 2405-2410. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, J.; Oliveira, S.C.A.; Oliveira, O.; Oliveira, F.A.; Oliveira, M.; Costales, C.; Ribeiro, F.; Pereira, O.F.; Oliveira, D.; Oliveira, A.R.; Imprinting imune, amplitude do reconhecimento de variantes, e resposta do centro germinal na infecção humana SARS-CoV-2 e vacinação. Cela 2022, 185, 1025–1040.e14. [Google Acadêmico] [Referência Cruzada]
- Comportamento da Proteína Spike. Disponível online: https://www.science.org/content/blog-post/spike-protein-behavior (acesso em 1º de outubro de 2022).
- Oliveira, A.; Oliveira, A.; Oliveira, M.; Kallen, J.-J.; Desenvolvimento de Tecnologias de Vacinas MRNA. RNA Biol. 2012, 9, 1319–1330. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.-B.; Oliveira, F.M.; van Hoof, A. Regulação do RNA mensageiro: traduzir ou degradar. EMBO J. 2008, 27, 471–481. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Oliveira, A.; Oliveira, E.C.; Ribeiro, F.; Oliveira, M.; Oliveira, A.; Oliveira, V.; Becskei, A. Controle Gênico Multiplexado Revela Rápido Turnover de MRNA. Adv. 2017, 3, e1700006. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Oliveira, E.; Oliveira, R.; Oliveira, E.; Pereira, A.; Ribeiro, C.; Oliveira, E.; Oliveira, J.; Oliveira, M.; Oliveira, R.V.; et al. Persistência da proteína S2 de SARS-CoV-1 em indivíduos pós-vacinação negativos de SARS-CoV-2 com sintomas longos de COVID/PASC-like. Res. Sq. 2022, Preprint. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.B.; Oliveira, E.B.; Oliveira, R.; Oliveira, E.; Pereira, A.; Rodrigues, H.; Oliveira, E.; Oliveira, M.; Pereira, P.; Oliveira, J.; et al. Persistência da proteína SARS CoV-2 S1 em monócitos CD16+ em sequelas pós-agudas de COVID-19 (PASC) até 15 meses pós-infecção. Frente. Imunol. 2022, 12, 5526. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Oliveira, M.S.; Oliveira, C.; Oliveira, J.W.; Oliveira, C.R.; Zaki, H. A proteína spike do SARS-CoV-2 induz a inflamação através da activação dependente de TLR2 da via NF-ΚB. Elife 2021, 10, e68563. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.P.; Oliveira, M.; Oliveira, E.; Siqueiros-Márquez, L.; Martinez de la Escalera, G.; Ribeiro, C.; A proteína spike do SARS-CoV-2 induz a inflamação endotelial através da sinalização da integrina A5β1 e NF-ΚB. J. Biol. 2022, 298 101695. [Google Acadêmico] [Referência Cruzada]
- Oliveira, W.A.; Oliveira, P.; Oliveira, J.M.; Pereira, J.M.; Oliveira, N.; Whiteside, T.L. Transporte de vesículas extracelulares através da barreira hematoencefálica: farmacocinética cerebral e efeitos da inflamação. Int. J. Mol. 2020, 21, 4407. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.A.; Oliveira, A.M.; Oliveira, P.; Ribeiro, J.V.; Chan, W.C.W. Taxa de fluxo afeta a captação de nanopartículas em células endoteliais. Adv. Mater. 2020, 32, e1906274. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, J.P.; Oliveira, J.B.; Ribeiro, A.; Oliveira, A.A.; Oliveira, A.M.; Oliveira, J.A.; Ribeiro, R.; Pereira, J.F.; Oliveira, A.A.; Ribeiro, R.; et al. A proteína spike do SARS-CoV-2 altera a função de barreira em modelos 2D estáticos e 3D microfluídicos in vitro da barreira hematoencefálica humana. Neurobiol. 2020, 146, 105131. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, L.; Oliveira, I.; Oliveira, J.; Oliveira, C.H.; Oliveira, A.; Luchian, T. Permeabilização da membrana lipídica não-mediada pelo receptor pela subunidade S2 da proteína spike de SARS-CoV-1. ACS Appl. Mater. Interfaces 2020, 12, 55649–55658. [Google Acadêmico] [CrossRef] [PubMed]
- Malhotra, A. Curando a pandemia de desinformação sobre vacinas de MRNA COVID-19 através da medicina baseada em evidências reais – Parte 1. J. Insul. Resistir. 2022, 5, 8. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.R.; Ribeiro, R.; Duncanson, E. Achados cardíacos histopatológicos da autópsia em 2 adolescentes após a segunda dose da vacina COVID-19. Arco Pathol. Laboratório Med. 2022, 146, 925-929. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.G.; Pereira, G.T.; Oliveira, J.A.; Oliveira, A.R.; Oliveira, I.V.; Robicsek, A. Miocardite e pericardite após a vacinação para COVID-19. JAMA 2021, 326, 1210–1212. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, Ø.; Oliveira, P.; Oliveira, A.; Oliveira, A.; Oliveira, R.M.; Ribeiro, A.; Pereira, J.V.; Oliveira, A.; Oliveira, A.; Pereira, A.; Vacinação contra SARS-CoV-2 e miocardite em um estudo de coorte nórdico de 23 milhões de residentes. JAMA Cardiol. 2022, 7, 600–612. [Google Acadêmico] [Referência Cruzada]
- Oliveira, M.; Oliveira, J.A.; Pereira, L.; Oliveira, A.; Oliveira, F.; Ribeiro, M.; Oliveira, P.; Oliveira, J.; Oliveira, A.; Oliveira, C.A.C.; et al. Riscos de miocardite, pericardite e arritmias cardíacas associadas à vacinação COVID-19 ou infecção por SARS-CoV-2. Nat. 2022, 28, 410-422. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Oliveira, M.E.; Oliveira, A.R.; Oliveira, M.M.; Oliveira, M.; Escudos, K.; Ribeiro, C.B.; Oliveira, A.; Ribeiro, A.; Oliveira, J.; et al. Resultados pelo menos 90 dias desde o início da miocardite após a vacinação COVID-19 de MRNA em adolescentes e adultos jovens nos EUA: um estudo de vigilância de acompanhamento. Lancet Criança Adolescente. Saúde 2022, 6, 788–798. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, P.; Ribeiro, A.; Oliveira, A.; Ribeiro, A.; Mansanguan, C. Manifestação cardiovascular da vacina BNT162b2 MRNA COVID-19 em adolescentes. Infectar. 2022, 7, 196. [Google Acadêmico] [Referência Cruzada]
- Oliveira, W.; Oliveira, L.; Oliveira, A.; Ribeiro, J.; Oliveira, D.; Oliveira, A.; Oliveira, A.; Du, L. Caracterização do domínio de ligação do receptor (RBD) do novo coronavirus 2019: implicação para o desenvolvimento da proteína RBD como um inibidor da ligação viral e vacina. Célula Mol. 2020, 17, 613-620. [Google Acadêmico] [Referência Cruzada]
- Pereira, C.B.; Oliveira, M.; Oliveira, A.; Choe, H. Mecanismos da entrada de SARS-CoV-2 nas pilhas. Rev. Mol. 2022, 23, 3-20. [Google Acadêmico] [Referência Cruzada]
- Oliveira, Y.-H.; Oliveira, J.; Oliveira, J.; Pereira, J.J.; Oliveira, J.; Oliveira, J.; Oliveira, A.; Park, S.B. Inibição da interação ACE2-Spike por um ligante ACE2 suprime a entrada SARS-CoV-2. Angew. Chem. Int. Ed. 2022, 61, e202115695. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, D.; Oliveira, J.; Oliveira, A.; Aguirre-Sampieri, A.; Oliveira, A.; Vaca, L. Vacinas SARS-CoV-2 baseadas na glicoproteína spike e implicações de novas variantes virais. Frente. Imunol. 2021, 12, 701501. [Google Acadêmico] [CrossRef] [PubMed]
- Ler, A.F.; Oliveira, J.J.; Poderes, C.; Oliveira, A.B.; Oliveira, A.; Oliveira, J.P.; Oliveira, A.A.; Walkden-Brown, S.W.; Nair, V.K. A vacinação imperfeita pode aumentar a transmissão de patógenos altamente virulentos. PLoS Biol. 2015, 13, e1002198. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, F.P.; Pereira, C.T.; Oliveira, M.; Oliveira, E.L.; Oliveira, J.; Oliveira, C.H.; Oliveira, R.L.; Oliveira, J.G.; Ribeiro, M.; Pereira, R.N.; Transmissão domiciliar de SARS-CoV-2 Omicron variante de preocupação Subvariantes BA.1 e BA.2 na Dinamarca. Nat. 2022, 13, 5760. [Google Acadêmico] [Referência Cruzada]
- Oliveira, G.I.; Oliveira, M.; Oliveira, G.S.; Oliveira, F.A.; Oliveira, E.; José, M.V. Teste de evolução neutro da proteína spike do SARS-CoV-2 e suas implicações na ligação ao ACE2. Rep. 2021, 11, 18847. [Google Acadêmico] [Referência Cruzada]
- Oliveira, D.; Oliveira, P.; Pereira, M.; Oliveira, M.; Oliveira, A.S.; Kaur, P. Insights estruturais e funcionais nas mutações da proteína spike das variantes emergentes do SARS-CoV-2. Vida Sci. 2021, 78, 7967-7989. [Google Acadêmico] [Referência Cruzada]
- Oliveira, E.A.; Oliveira, L.; Oliveira, J.M.; Topol, E.J. Long COVID: Principais descobertas, mecanismos e recomendações. Rev. Microbiol. 2023, 21, 133-146. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Ribeiro, A.A.E.; Oliveira, A.M.; Oliveira, A.N.; Oliveira, J.; Oliveira, A.; Oliveira, A.; Sheikh, A.B. COVID-19 Vaccine e Long COVID: Uma revisão de escopo. Vida 2022, 12, 1066. [Google Acadêmico] [Referência Cruzada]
- Loh, E.-W. Estudo dose-resposta um material bruto rico em glicosídeo e rutinosídeo no alívio dos efeitos colaterais das vacinas COVID-19. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT05387252 (acesso em 30 de setembro de 2022).
- Universidade de Oxford. Caracterização dos efeitos da espermidina, um suplemento nutricional, na resposta da memória imunológica à vacina contra o coronavírus em pessoas idosas. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT05421546 (acesso em 30 de setembro de 2022).
- Universidade de Sherbrooke. Modulação das respostas imunes à vacinação COVID-19 por uma intervenção na microbiota intestinal: um ensaio clínico randomizado e controlado. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT05195151 (acesso em 30 de setembro de 2022).
- AB Biotek. Eficácia e tolerabilidade de uma suplementação nutricional com ABBC-1, uma combinação simbiótica de beta-glucanos e probióticos enriquecidos com selênio e zinco, em voluntários que recebem as vacinas contra a gripe ou COVID-19. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT04798677 (acesso em 30 de setembro de 2022).
- Centro Médico da Universidade de Maastricht. O efeito do consumo de éster de estanol vegetal na resposta vacinal a uma vacina COVID-19. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT04844346 (acesso em 30 de setembro de 2022).
- Saxe, G. Multicêntrico duplo-cego, Placebo-controlado RCT de Fomitopsis Officinalis/Trametes versicolor para COVID-19. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT04951336 (acesso em 30 de setembro de 2022).
- Engındenız, Z. Avaliação de exercícios do músculo deltoide no local da injeção e dor no braço após a vacinação de Pfizer-BioNTech (BNT162b2) COVID-19, um estudo controlado randomizado. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT05157230 (acesso em 30 de setembro de 2022).
- Sanchez, J. Aumento da resposta imune à vacinação COVID-19 MRNA através do tratamento manipulativo osteopático incluindo bombas linfáticas. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT04928456 (acesso em 30 de setembro de 2022).
- Universidade de Rowan. Medicina Osteopática Linfática Manipulativa para Aumentar a Eficácia da Vacinação COVID-19. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT05069636 (acesso em 30 de setembro de 2022).
- Bartley, J. Eficácia da vacinação com metformina em adultos mais velhos: um estudo piloto. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT03996538 (acesso em 30 de setembro de 2022).
- Karanja, P.S. Ferro e Doença Viral Imunoprevenível. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT04912661 (acesso em 30 de setembro de 2022).
- Matéria Médica Holding. Ensaio clínico multicêntrico, duplo-cego, controlado por placebo, randomizado, de grupo paralelo para avaliar a eficácia e a segurança de Ergoferon como prevenção COVID-19 não específica durante a vacinação contra o SARS-CoV-2. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT05069649 (acesso em 30 de setembro de 2022).
- Gnessi, L. Vacinação COVID-19 em indivíduos com obesidade: impacto da saúde metabólica e o papel de uma dieta cetogênica. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT05163743 (acesso em 30 de setembro de 2022).
- Wang, A.X. Impacto do ajuste da imunossupressão na resposta imune à vacinação de MRNA SARS-CoV-2 em receptores de transplante renal (ADIVKT). 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT05060991 (acesso em 30 de setembro de 2022).
- Hospital Universitário Inselspital, Berna. Estudo de registro para a eficácia da vacinação COVID19 em pacientes com histórico de tratamento de rituximabe. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT04877496 (acesso em 30 de setembro de 2022).
- Oliveira, J.E.; Oliveira, L.; Oliveira, A.; Oliveira, C.; Oliveira, C.; Burton, M.J. Intervenções para a prevenção da disfunção olfativa persistente pós-COVID-19. Banco de Dados Cochrane Syst. Rev. 2021, 2021, CD013877. [Google Acadêmico] [Referência Cruzada]
- Pereira, E.A.; Oliveira, L.; Oliveira, D.S.; Ribeiro, V.-S.; Oliveira, V.B.; Ribeiro, E.; Ribeiro, G.; Oliveira, M.; Pereira, A.; Oliveira, E.M.; et al. O MRNA da vacina pode ser detectado no sangue 15 dias após a vacinação. Biomedicamentos 2022, 10, 1538. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Oliveira, J.J.; Oliveira, O.; Ribeiro, A.; Oliveira, A.A.; Oliveira, J.J.; Oliveira, E.M.; Oliveira, M.; Oliveira, Ö.; Oliveira, J.; et al. Demonstração Pré-Clínica e Clínica da Imunogenicidade por Vacinas MRNA contra os Vírus Influenza H10N8 e H7N9. Mol. 2017, 25, 1316–1327. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Oliveira, A.; Pereira, A.; Oliveira, C.; Oliveira, A.; Oliveira, E.; Nayak, A. Detecção de vacinas COVID-19 do RNA mensageiro no leite materno humano. JAMA Pediatr. 2022, 176, 1268. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.G.; Oliveira, C.; Oliveira, A.; Oliveira, A.; Oliveira, D.; Oliveira, A.; Oliveira, B.; Oliveira, J.-J.; Oliveira, B.; Tili, E. Dano da pilha endotelial é a parte central de COVID-19 e um modelo do rato induzido pela injecção da subunidade S1 da proteína spike. Ana Diagn. Pathol. 2021, 51, 151682. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Oliveira, D.B.; Leo, M.D. A PROTEÍNA SPIKE SARS-CoV-2 induz a degradação de proteínas juncionais que mantêm a integridade da barreira endotelial. Frente. Cardiovasc. Med. 2021, 8, 687783. [Google Acadêmico] [CrossRef] [PubMed]
- Pereira, A.; Oliveira, J.; Oliveira, C.R.; Oliveira, M.; Oliveira, A.; Pereira, A.; Oliveira, A.; Ribeiro, A.; Oliveira, A.; Oliveira, L.; A proteína spike do SARS-CoV-2 prejudica a função endotelial via downregulation da ECA 2. Circ. 2021, 128, 1323-1326. [Google Acadêmico] [Referência Cruzada]
- Oliveira, C.; Oliveira, A.; Oliveira, M.E.; Ribeiro, M.; Ribeiro, G.; A influência das vacinas de MRNA COVID-19-baseadas em medidas da artéria do conduto e da função endotelial microvascular. FASEB J. 2022, 36. [Google Acadêmico] [Referência Cruzada]
- Oliveira, D.; Oliveira, P.; Oliveira, A.; Oliveira, M.; Oliveira, J.; Oliveira, C.; Ribeiro, C.; Oliveira, I.; Van den Heede, K. Fisiopatologia e mecanismo de COVID longo: uma revisão abrangente. Ann. Med. 2022, 54, 1473-1487. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, H.; Oliveira, A.; Oliveira, J.; Oliveira, M.; Edison, P. Mecanismos de Covid longa, fatores de risco e manejo. BMJ 2021, 374, n1648. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, E.; Oliveira, A.; Al-Aly, Z. Resultados cardiovasculares de longo prazo de COVID-19. Nat. 2022, 28, 583-590. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.A.; Oliveira, F.F.; Neubauer, S. COVID longo: sequelas pós-agudas de COVID-19 com um foco cardiovascular. Eur. Coração J. 2022, 43, 1157-1172. [Google Acadêmico] [Referência Cruzada]
- Oliveira, M.M.; Oliveira, Z.; Oliveira, A.C.; Queimaduras, M.D.; Oliveira, A.; Ribeiro, A.P.; Oliveira, J.P.; Oliveira, M.; Oliveira, A.; Oliveira, A.; Proteína spike circulante detectada na miocardite da vacina MRNA pós-COVID-19. Circulação 2023, 147, 867–876. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Oliveira, A.; Ribeiro, A.; Oliveira, A.; Oliveira, A.; Oliveira, M.; Oliveira, X.; Oliveira, A.; Ribeiro, A.; SARS-CoV-2 liga a plaqueta ACE2 para aumentar a trombose em COVID-19. J. Hematol. Oncol. 2020, 13, 120. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.M.; Ribeiro, C.; Oliveira, M.; Oliveira, M.; Oliveira, J.G.; Oliveira, J.J.; Oliveira, J.; Oliveira, D.B.; Pretorius, E. SARS-CoV-2 Spike Protein S1 induz fibrina (Ogen) resistente à fibrinólise: implicações para a formação de microcoágulos em COVID-19. Rep. 2021, 41, BSR20210611. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, A.; Hammarström, P. Amiloidogênese da proteína spike de SARS-CoV-2. J. Am. Chem. 2022, 144, 8945-8950. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Ribeiro, M.; Oliveira, R.; Oliveira, D.; Ribeiro, A.; Oliveira, L.; Oliveira, D.; Oliveira, D.; Oliveira, K.; Ribeiro, M.; Miocardite após imunização com vacinas MRNA COVID-19 em membros das forças armadas dos EUA. JAMA Cardiol. 2021, 6, 1202-1206. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, C.; Ribeiro, M.; Sharma, A.R. Apresentam variantes de preocupação e variantes de interesse do coronavírus 2 da Síndrome Respiratória Aguda Grave: suas mutações significativas na glicoproteína S, infectividade, reinfectividade, escape imunológico e atividade vacinal. Rev. Med. 2022, 32, e2270. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.A.; Oliveira, A.M.; Pereira, A.; Ribeiro, J.R.; Oliveira, A.C.; Ribeiro, E.M.; Oliveira, C.; Ribeiro, R.; Ribeiro, A.; Oliveira, J.J.; Variantes do SARS-CoV-2, mutações spike e escape imunológico. Rev. Microbiol. 2021, 19, 409-424. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.Y.; Pereira, J.; Oliveira, P.A.; Oliveira, J.; Oliveira, J.; Ribeiro, A.A.; Oliveira, L.; Oliveira, M.; Oliveira, E.; Oliveira, A.; et al. Imunogenicidade dos reforços da vacina BA.5 bivalente contra MRNA. N. Engl. J. Med. 2023, 388, 565-567. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, J.-H.; Oliveira, A.; Ribeiro, R.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, J.; Pereira, A.D.; Oliveira, J.; Oliveira, M.; SARS-CoV-2 Spike Glycoprotein Vaccine Candidate NVX-CoV2373 Imunogenicidade em babuínos e proteção em camundongos. Nat. 2021, 12, 372. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, C.; Oliveira, A.R.; Ribeiro, M.; Lee, S.-S. Uma visão detalhada do escape imune, escape do anticorpo, escape parcial da vacina do SARS-CoV-2 e suas variantes emergentes com mutações do escape. Frente. Imunol. 2022, 13, 801522. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, J.; Oliveira, A.; Oliveira, W.; Oliveira, J.; Oliveira, A.; Oliveira, L.; Oliveira, A.; Oliveira, J.; Oliveira, Z.; Mecanismo molecular para o aumento dependente de anticorpos da entrada do coronavírus. J. Virol. 2020, 94, e02015-19. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, G.; Oliveira, A.; Oliveira, M.; Oliveira, M.; Pereira, V.; Oliveira, A.; Oliveira, L.; Oliveira, J.; Pereira, C.; Ribeiro, R.; et al. Eficácia de uma quarta dose da vacina COVID-19 MRNA contra Omicron. N. Engl. J. Med. 2022, 386, 1377-1380. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Oliveira, J.; Oliveira, J.; Oliveira, A.; Oliveira, A.; Oliveira, C.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, R.; Investigações abrangentes revelaram alterações fisiopatológicas consistentes após a vacinação com vacinas COVID-19. Disco celular. 2021, 7, 99. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Pereira, J.J.; Oliveira, D.; Ribeiro, M.; Ribeiro, M.; Oliveira, A.; Oliveira, A.; Oliveira, M.; Oliveira, A.; Oliveira, H.; Comprometimento de múltiplos órgãos e COVID longo: um estudo de coorte longitudinal prospectivo de 1 ano. J. R. Soc. 2023, 116, 97–112. [Google Acadêmico] [Referência Cruzada]
- Mustafá Alhussein, M.; Ribeiro, M.; Oliveira, A.; Oliveira, A.; Ribeiro, D.; Oliveira, J.; Oliveira, C.P.; Oliveira, A.G.; Oliveira, A.; Oliveira, A.; História natural da lesão miocárdica após miocardite associada à vacina COVID-19. Cân. J. Cardiol. 2022, 38, 1676-1683. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, M.G.; Oliveira, Z.; Oliveira, M.; Oliveira, O.; Oliveira, A.; Oliveira, R.; Oliveira, G.; Cavaleiro, R.; Oliveira, M.; Oliveira, D.L.H.; Neuropatia aguda de fibras pequenas após vacinação com Oxford-AstraZeneca ChAdOx1-S: relato de três casos e revisão da literatura. J. Peripher. Nerv. Syst. 2022, 27, 325-329. [Google Acadêmico] [Referência Cruzada]
- Oliveira, F.; Oliveira, A.; Oliveira, Z.; Yu, J. Neuropatia de fibra pequena associada com a vacina SARS-CoV-2 da Moderna. Cura 2022, 14, e25969. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.A.; Oliveira, A.A.; Oliveira, M.F.; Oliveira, D.; Oliveira, A.; Oliveira, A.; Yusof Khan, A.H.K.; Santacatterina, M.; Oliveira, J.; Oliveira, J.T.; Eventos neurológicos relatados após vacinas COVID-19: uma análise do sistema de notificação de eventos adversos de vacinas. Ana Neurol. 2022, 91, 756-771. [Google Acadêmico] [Referência Cruzada]
- Oliveira, D.; Oliveira, C.; Pouwels, K.B.; Oliveira, M.; Oliveira, V.; Oliveira, F.; Oliveira, J.; Oliveira, A.A.; Walker, A.S. Trajetória dos sintomas longos da Covid após a vacinação COVID-19: estudo de coorte baseado na comunidade. BMJ 2022, 377, e069676. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, C.; Oliveira, M.M.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Schirmacher, P. Caracterização histopatológica baseada em autópsia de miocardite após vacinação anti-SARS-CoV-2. Clin. Res. Cardiol. 2023, 112, 431-440. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.G.; Oliveira, J.; Oliveira, R.; Oliveira, P.L.; Oliveira, A.; Ribeiro, P.; Pereira, E.A.; Oliveira, M.M.; Pereira, R.A.; Oliveira, A.M.; et al. Segurança das vacinas de MRNA administradas durante os 6 meses iniciais do programa de vacinação COVID-19 dos EUA: um estudo observacional de relatórios para o sistema de notificação de eventos adversos da vacina e v-safe. Lancet Infect. 2022, 22, 802-812. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.A.; Oliveira, A.L.; Oliveira, A.; Oliveira, J.E.; Sábio, J.K.; Oliveira, J.M.; Pereira, R.B.; Oliveira, D.R.; Oliveira, J.M.; Oliveira, A.; Segurança comparativa das vacinas BNT162b2 e MRNA-1273 em uma coorte nacional de veteranos dos EUA. Estagiária do JAMA. 2022, 182, 739-746. [Google Acadêmico] [Referência Cruzada]
- Oliveira, G.; Oliveira, L.; Oliveira, M.; Oliveira, A.; Oliveira, G.; Oliveira, A.; Oliveira, R.; Tomasi, A. COVID-19 Espalhando-se pelo mundo correlaciona-se com o alelo C677T da prevalência do gene da metilenotetrahidrofolato redutase (MTHFR). J. Clin. 2021, 35, 23798, e<>. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, G.; Oliveira, D.; Henrique, A.M.; Oliveira, M.; Lippi, G. Homocisteína na doença do coronavirus (COVID-19): uma revisão sistemática da literatura. Diagnóstico 2022, 9, 306–310. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, G.; Oliveira, A.; Oliveira, G.; Oliveira, M.; Oliveira, A.; Oliveira, A.; Oliveira, R.; Oliveira, A.; Oliveira, A.; Ribeiro, G.; Avaliação da homocisteína (Hcy) para prever resultados de pacientes COVID-19 hospitalizados: um estudo multicêntrico em 313 pacientes COVID-19. Clin. 2021, 59, e354–e357. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, M.; Oliveira, A.; Oliveira, M.M.; Oliveira, P.; Oliveira, A.M.; Oliveira, E.A.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Marcadores genéticos prognósticos para trombose em pacientes com COVID-19: uma análise focada em dímero D, homocisteína e tromboembolismo. Pharm frontal. 2020, 11, 587451. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, M.; Pereira, J.; Achenbach, J. Curso com risco de vida na doença do coronavirus 2019 (COVID-19): Existe uma ligação com o polimorfismo da metilenotetrahidrofólica redutase (MTHFR) e hiper-homocisteinemia? Hipóteses 2020, 144, 110234. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Ribeiro, M.B.; Ribeiro, J.T.; Todos os frascos não são iguais: papel potencial da qualidade da vacina nas reações adversas da vacina. Vacina 2021, 39, 6565–6569. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, J.A.; Oliveira, A.C.; Oliveira, A.S.; Oliveira, J.F.; Oliveira, A.; Gordon, S.M. Eficácia da Vacina Bivalente da Doença do Coronavirus 2019 (COVID-19). medRxiv 2023. [Google Acadêmico] [Referência Cruzada]
- Oliveira, M.A.; Pereira, J.J.; Ribeiro, P.; Ribeiro, A.-G.; Plachter, B. Avaliação de dados graduados por idade e sexo de reações vacinais após a injeção inicial da vacina BNT162b2 MRNA em um centro de vacinação local na Alemanha. Vacinas 2021, 9, 911. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, P.; Oliveira, C.S.; Oliveira, J.L.; Pereira, L.A.; Oliveira, R.R.; Oliveira, J.J.; Oliveira, F.; Os efeitos inespecíficos e diferenciais por sexo das vacinas. Rev. Imunol. 2020, 20, 464-470. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.P.; Oliveira, A.P.; Loomis, G.J. Relação entre alergias pré-existentes e reações anafiláticas após a administração da vacina COVID-19 de MRNA. Vacina 2021, 39, 4407–4409. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, E.-J.; Oliveira, M.; Oliveira, A.; Pereira, A.; Ribeiro, J.; Oliveira, A.; Oliveira, A.; Oliveira, C.; Oliveira, C.; Oliveira, A.D.; Vacinação contra SARS-CoV-2 e PTI em pacientes com PTI de novo ou preexistente. Sangue 2022, 139, 1564–1574. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, M.; Oliveira, A.; Ribeiro, G.; Fernandez Del Campo, S.S.; Oliveira, A.; Oliveira, R.M.; Bohn, T. Fortalecendo o sistema imunológico e reduzindo a inflamação e o estresse oxidativo através da dieta e nutrição: considerações durante a crise COVID-19. Nutrientes 2020, 12, 1562. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, M.; Oliveira, R.; Oliveira, P.; Oliveira, A.; Pereira, P.; Oliveira, C.; Oliveira, J.M.; Oliveira, A.; Pereira, M.; Oliveira, J.; et al. O impacto da obesidade nas complicações COVID-19: um estudo de coorte retrospectivo. Int. J. Obes. 2020, 44, 1832-1837. [Google Acadêmico] [Referência Cruzada]
- Oliveira, M.; Oliveira, M.C.; Oliveira, M.; Oliveira, A.; Oliveira, A.; Del Prato, S. COVID-19 em pessoas com diabetes: entendendo as razões para piores resultados. Lancet Diabetes Endocrinol. 2020, 8, 782-792. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, E.; Oliveira, C.; Oliveira, C.; Ribeiro, E.; Oliveira, J.S.; Oliveira, F.; Oliveira, M.F.; Oliveira, C.; Ribeiro, M.; Oliveira, E.; et al. Uma visão gerada por máquina do papel dos níveis de glicose no sangue na gravidade da COVID-19. Frente. Saúde Pública 2021, 9, 695139. [Google Acadêmico] [CrossRef] [PubMed]
- Pereira, E.M.; Oliveira, A.M.; Oliveira, A.; Oliveira, A.; Oliveira, J.; Oliveira, J.A.; Oliveira, C.-P.; Sinaiko, A.R. Consumo de frutas e hortaliças e sua relação com marcadores de inflamação e estresse oxidativo em adolescentes. J. Am. Dieta. 2009, 109, 414–421. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.-C.; Oliveira, J.-M.; Oliveira, J.L.; Hung, Y.-C. Polifenóis e estresse oxidativo na doença isquêmica do coração relacionada à aterosclerose e acidente vascular cerebral. Célula Oxidativa Med. Longev. 2017, 2017, 8526438. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Salazar, G. Papel protetor dos polifenóis contra inflamação vascular, envelhecimento e doença cardiovascular. Nutrientes 2018, 11, 53. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Mão, T.W. Papel da Microbiota na Imunidade e Inflamação. Cela 2014, 157, 121–141. [Google Acadêmico] [CrossRef] [PubMed]
- Sim, Y.K.; Oliveira, A.; Oliveira, G.C.-Y.; Oliveira, F.; Oliveira, A.; Oliveira, A.A.; Pereira, A.C.; Pereira, C.P.; Oliveira, E.J.; Oliveira, A.C.; A composição da microbiota intestinal reflete a gravidade da doença e as respostas imunes disfuncionais em pacientes com COVID-19. Intestino 2021, 70, 698–706. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Oliveira, F.; Oliveira, G.; Oliveira, E.; Sim, Y.K.; Oliveira, Z.; Oliveira, A.; Oliveira, F.K.L.; Pereira, P.; et al. Representando a actividade viral fecal SARS-CoV-2 em associação com a composição da microbiota intestinal em pacientes com COVID-19. Intestino 2021, 70, 276–284. [Google Acadêmico] [CrossRef] [PubMed]
- Ferreira, C.; Oliveira, D.A.; Reis, F. Disbiose da microbiota intestinal – Hiperresposta imune – Tríade de inflamação na doença do coronavirus 2019 (COVID-19): Impacto das abordagens farmacológicas e nutracêuticas. Microrganismos 2020, 8, 1514. [Google Acadêmico] [Referência Cruzada]
- Oliveira, C.; Ribeiro, R.; Oliveira, J.; Oliveira, W.; Oliveira, M.N.A.; Oliveira, A.; Pereira, A.; Ribeiro, A.; Fernandez-Delgado, R.; Oliveira, A.; et al. Um local imunogênico conservado e vulnerável na proteína spike do coronavírus delineado por anticorpos monoclonais reativos cruzados. Nat. 2021, 12, 1715. [Google Acadêmico] [Referência Cruzada]
- Li, F. Estrutura, Função e Evolução das Proteínas Spike do Coronavírus. Rev. Virol. 2016, 3, 237–261. [Google Acadêmico] [CrossRef] [PubMed]
- Pollard, T.D. Um Guia para Ensaios de Vinculação Simples e Informativos. Célula 2010, 21, 4061–4067. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Kehn-Hall, K. Determinação da concentração viral através de ensaios de placa: usando sistemas de sobreposição tradicionais e novos. J. Vis. 2014, 52065. [Google Acadêmico] [Referência Cruzada]
- Pereira, A.; Oliveira, J.L.; Oliveira, A.C.; Oliveira, D.M.; Domingo, G.J. Operações de laboratório, processamento e manuseio de amostras para testes de carga viral e vigilância. J. Infectar. 2010, 201 (Suppl. 1), S27–S36. [Google Acadêmico] [Referência Cruzada]
- Gillette, J.R. Problemas na correlação de estudos InVitro e InVivo do metabolismo de drogas. In Farmacocinética: Uma Visão Moderna; Benet, L.Z., Levy, G., Ferraiolo, B.L., Eds.; Springer: Boston, MA, EUA, 1984; pp. 235-252. ISBN 978-1-4613-2799-8. [Google Acadêmico]
- Oliveira, D.; Schaefer, S.T. Ensaios clínicos randomizados vs. estudos observacionais: por que não apenas viver juntos? BMC Anesth. 2016, 16, 102. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, M.S.; Oliveira, A.; Ribeiro, A.; Oliveira, I.; Elshazly, S.; Uma atualização sobre a síndrome de trombocitopenia trombótica induzida pela vacina COVID-19 e algumas recomendações de manejo. Moléculas 2021, 26, 5004. [Google Acadêmico] [Referência Cruzada]
- Oliveira, G.; Oliveira, F.; Kwiatkowska, A.; O caminho para inibidores terapêuticos de furina: de feromônios de levedura a SARS-CoV-2. Int. J. Mol. 2022, 23, 3435. [Google Acadêmico] [Referência Cruzada]
- Oliveira, Y.-W.; Ribeiro, J.-L.; Oliveira, C.-L.; Oliveira, M.-F.; Oliveira, A.-C.; Oliveira, A.-H.; Ribeiro, Y.-H.; Pereira, C.-A.; Oliveira, A.-M.; Pereira, A.-A.; Os inibidores de furina bloqueiam a clivagem da proteína spike do SARS-CoV-2 para suprimir a produção do vírus e os efeitos citopáticos. Rep. Celular 2020, 33, 108254. [Google Acadêmico] [Referência Cruzada]
- Oliveira, C.; Oliveira, M.; Ribeiro, A.; Oliveira, X.; Ribeiro, K.; Oliveira, M.; Oliveira, A.; Oliveira, A.; Oliveira, P.; Oliveira, A.; Furin: Um alvo terapêutico potencial para COVID-19. iScience 2020, 23, 101642. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.Z.; Pereira, I.T.; Ribeiro, A.; Ribeiro, D.; Fernandes, P.B.; Ribeiro, J.R.; Oliveira, M.M.; Haagmans, B.L. A ENTRADA DO SARS-CoV-2 nos organoides das vias aéreas humanas é mediada por serina protease e facilitada pelo sítio de clivagem multibásico. eLife 2021, 10, e64508. [Google Acadêmico] [Referência Cruzada]
- Oliveira, E.; Oliveira, A.E.; Oliveira, M.; Oliveira, D.; Frängsmyr, L.; Pereira, B.D.; Ribeiro, D.G.; Oliveira, R.; Ribeiro, J.; Oliveira, M.; Os inibidores de protease serina restringem a suscetibilidade do hospedeiro a infecções por SARS-CoV-2. mBio 2022, 13, e0089222. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Sargento, T.; Oliveira, G.; Oliveira, J.; Perlman, A.; Ribeiro, T.; Uma serina protease transmembrana está ligada ao receptor do coronavírus da síndrome respiratória aguda grave e ativa a entrada do vírus. J. Virol. 2011, 85, 873–882. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, J.; Oliveira, A.; Ribeiro, A.; Oliveira, H.; Wang, C. Drogas antipsicóticas rastreadas inibem a ligação do SARS-CoV-2 com ACE2 in Vitro. Vida Sci. 2021, 266, 118889. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, J.; Oliveira, A.; Oliveira, A.M.; Oliveira, Z.; Oliveira, G.; Liu, P. Lenalidomida downregulates ACE2 abundância de proteína para aliviar a infecção por SARS-CoV-2 proteína spike condicionada pseudovírus. Transduto de Sinais. Alvo. Ther. 2021, 6, 186. [Google Acadêmico] [Referência Cruzada]
- Ramadã, A.A.; Oliveira, J.; Oliveira, A.R.; Oliveira, A.; Oliveira, M.A.; Oliveira, M.M.; Oliveira, A.S.; Oliveira, A.; Oliveira, A.; Oliveira, J.J.; et al. A inibição da palmitoilação da proteína spike do SARS-CoV-2 reduz a infectividade do vírus. bioRxiv 2021. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Oliveira, A.; Oliveira, A.; Ribeiro, A.; Oliveira, A.; Oliveira, J.J.; Ribeiro, M.S. Um peptídeo terapêutico novo bloqueia a ligação da proteína spike do SARS-CoV-2 com o receptor ACE2 da pilha hospedeira. Drogas P&D 2021, 21, 273–283. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.B.; Oliveira, J.L.; McCracken, A.A. Autofagia: Um Processo de Controle de Qualidade de Proteínas ER. Autofagia 2006, 2, 135–137. [Google Acadêmico] [Referência Cruzada]
- Oliveira, R.; Dutta, S. Papel do microbioma na patogênese da COVID-19. Frente. Infectar células. Microbiol. 2022, 12, 736397. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, J.R.; Ribeiro, A.; Oliveira, A.; Oliveira, R.; Tleyjeh, I.M. Desvendando o mistério em torno das sequelas pós-agudas da COVID-19. Frente. Imunol. 2021, 12, 686029. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.P.; Pereira, E.; Oliveira, A.L.; Oliveira, L.; Oliveira, M.-C.; Oliveira, P.; Mutaawe, A.; Oliveira, O.; Oliveira, M.; Oliveira, A.M.; Disbiose do tipo inflamação do microbioma oral associa-se com a duração dos sintomas de COVID-19 e COVID longo. Insight JCI 2021, 6, e152346. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.D.; VanElzakker, M.B. COVID longo ou sequelas pós-agudas de COVID-19 (PASC): Uma visão geral dos factores biológicos que podem contribuir para sintomas persistentes. Frente. Microbiol. 2021, 12, 698169. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Oliveira, A.A.; Oliveira, A.; Oliveira, J.A.; Oliveira, J.; Ribeiro, B.D.; Oliveira, E.M.; Borody, T.J. Micróbios perdidos de COVID-19: Bifidobacterium, Depleção de Faecalibacterium e diversidade diminuída do microbiome associada com a gravidade da infecção SARS-CoV-2. BMJ Aberto Gastroenterol. 2022, 9, e000871. [Google Acadêmico] [Referência Cruzada]
- Gutiérrez-Castrellón, P.; Oliveira, A.; Abreu Y Abreu, A.T.; Ribeiro, D.C.; Oliveira, E.; Oliveira, A.; Oliveira, C.; López-Velázquez, G.; Espadaler-Mazo, J. Probiótico melhora a depuração sintomática e viral em pacientes ambulatoriais de Covid19: Um ensaio clínico randomizado, quádruplo-cego, controlado por placebo. Micróbios intestinais 2022, 14, 2018899. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, D.; Oliveira, J.; Oliveira, J.-R.; Ribeiro, A.; Oliveira, A.; Oliveira, J.-J.; Acompanhamento de seis meses da riqueza da microbiota intestinal em pacientes com COVID-19. Gut 2022, 71, 222–225. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, X.; Oliveira, A.; Lan, P. Alterações do microbioma intestinal em COVID-19. Genom. Proteom. Bioinforme. 2021, 19, 679-688. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Hayashida, K. Fatores modificáveis do anfitrião para a prevenção e o tratamento de COVID-19: dieta e estilo de vida/dieta e fatores de estilo de vida na prevenção de COVID-19. Nutrientes 2022, 14, 1876. [Google Acadêmico] [Referência Cruzada]
- Pereira, J.N.; Pereira, M.N.; Ribeiro, M.; Pereira, J.N.; Pereira, J.W.; A idade jovem e a hipótese da dieta baseada em plantas para a infecção SARS-CoV-2 baixa e a pandemia COVID-19 na África subsaariana. Alimentos Vegetais Hum. 2021, 76, 270-280. [Google Acadêmico] [Referência Cruzada]
- Brown, R.B. Baixo sódio dietético potencialmente medeia a prevenção COVID-19 associada com dietas à base de plantas integrais. Irmão J. Nutr. 2022, 129, 1136-1141. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Ribeiro, C.M.; Pereira, A.; Oliveira, C.; Oliveira, M.; Oliveira, J.F.; Oliveira, A.; Seidelmann, S.B. Dietas à base de plantas, dietas pescarianas e gravidade COVID-19: um estudo de caso-controle de base populacional em seis países. BMJ Nutr. Prev. Saúde 2021, 4, 257–266. [Google Acadêmico] [Referência Cruzada]
- Oliveira, D.; Oliveira, C.; Brown, A. Impacto do consumo de uma bebida láctea contendo um probiótico no humor e cognição. Eur. J. Clin. Nutr. 2007, 61, 355–361. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, M.; Lanzotti, V. Produtos de sementes de chia: uma visão geral. Rev. 2017, 16, 745–760. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.-H.; Oliveira, A.; Oliveira, F.; Oliveira, Z.-M.; Oliveira, Y.-H.; Oliveira, M.; Oliveira, F.; Oliveira, Z.; Yang, Y. Efeitos protetores do glucomanano de Konjac no microbioma intestinal com perturbação antibiótica em camundongos. Carbohidr. Pólipo. 2022, 290, 119476. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Ribeiro, A.; Oliveira, G.; Oliveira, P.; Pereira, A.; Zhong, G. Complexidade estrutural do glucomanano de konjac e seus derivados governa a diversidade e os resultados da microbiota intestinal. Carbohidr. Pólipo. 2022, 292, 119639. [Google Acadêmico] [Referência Cruzada]
- Oliveira, R.; Oliveira, J.; Pereira, R.; Oliveira, A.; Oliveira, M.; A influência de uma mistura de lactobacilo probiótico e inulina prebiótica na duração e gravidade dos sintomas entre indivíduos com COVID-19. Infectar. Tratar. 2021, 5, 1-12. [Google Acadêmico]
- Oliveira, A.C.; Pereira, J.G.; Pereira, D.; Oliveira, D.; Oliveira, D.B.; Oliveira, F.B.; Ribeiro, M.; Oliveira, C.G.; Oliveira, V.A.; Pereira, A.; Dietas direcionadas para microbiota intestinal modulam o estado imunológico humano. Cela 2021, 184, 4137–4153.e14. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.G.; Ribeiro, O.; Oliveira, E.; Oliveira, A.; Midulla, F. Diferenças e semelhanças entre SARS-CoV e SARS-CoV-2: Reconhecimento do domínio de ligação do receptor spike e infecção da pilha do anfitrião com o suporte de proteases de serina celular. Infecção 2020, 48, 665–669. [Google Acadêmico] [Referência Cruzada]
- Pereira, E.; Oliveira, M.; Go, E.U.; Oliveira, D.H.; Oliveira, A.; Oliveira, F.; Pereira, M.; Oliveira, A.A.; Simonsen, L. Comparando SARS-CoV-2 com SARS-CoV e pandemias de gripe. Lancet Infect. 2020, 20, e238–e244. [Google Acadêmico] [Referência Cruzada]
- Oliveira, M.; Oliveira, A.; Pöhlmann, S.; Um local de clivagem multibásico na proteína spike do SARS-CoV-2 é essencial para a infecção de células pulmonares humanas. Cela 2020, 78, 779–784.e5. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, C.; Oliveira, X.; Oliveira, A.; Oliveira, J.G.; Decroly, E.; A glicoproteína spike do novo coronavírus 2019-NCoV contém um local de clivagem semelhante a furina ausente no CoV do mesmo clado. Antivir. 2020, 176, 104742. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, M.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Ribeiro, A.; Oliveira, A.A.; Oliveira, G.; Oliveira, A.-A.; Oliveira, A.; A entrada da pilha SARS-CoV-2 depende de ACE2 e TMPRSS2 e é bloqueada por um inibidor da protease clinicamente comprovado. Cela 2020, 181, 271–280.e8. [Google Acadêmico] [CrossRef] [PubMed]
- Pereira, A.; Ribeiro, A.; Kulamadayil-Heidenreich, N.S.A.; Oliveira, A.; Oliveira, J.J.; Oliveira, C.; Oliveira, A.; Oliveira, M.; Wilkens, L.; Primeiro caso de estudo post-mortem em um paciente vacinado contra SARS-CoV-2. Int. J. Infect. 2021, 107, 172-175. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, F.P.; Oliveira, J.J.; Oliveira, A.; Ribeiro, J.; Oliveira, A.; Oliveira, A.; Pereira, J.L.; Oliveira, G.; Moreira, E.D.; Ribeiro, C.; et al. Segurança e eficácia da vacina BNT162b2 MRNA COVID-19. N. Engl. J. Med. 2020, 383, 2603-2615. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.A.; Oliveira, A.; Faltas, K.E.; Oliveira, J.R.; Oliveira, A.; Oliveira, A.P.; Oliveira, A.; Oliveira, A.; Oliveira, J.A.; Oliveira, M.; et al. Avaliação da vacina MRNA-1273 contra SARS-CoV-2 em primatas não humanos. N. Engl. J. Med. 2020, 383, 1544-1555. [Google Acadêmico] [Referência Cruzada]
- Oliveira, R.; Ribeiro, A.; Ribeiro, J.E.M.; Ribeiro, J.M.; Oliveira, G.; Oliveira, F.; Oliveira, D.; Oliveira, A.H.; Oliveira, A.; Oliveira, A.; A vacina COVID-26 baseada no vetor de Ad19 que codifica um imunógeno spike do SARS-CoV-2 estabilizado da pré-fusão induz respostas imunes humorais e celulares potentes. Npj Vacinas 2020, 5, 91. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, G.; Pereira, A.L.; Oliveira, A.; Oliveira, D.; Oliveira, A.; Oliveira, J.L.; Ribeiro, J.K.; Oliveira, J.-H.; Pereira, A.D.; Análise estrutural da proteína spike SARS-CoV-2 de comprimento total de uma candidata avançada da vacina. Ciência 2020, 370, 1089–1094. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Oliveira, A.; Oliveira, J.A.; Ribeiro, D.; Kirchdoerfer, R.N.; Pereira, A.L.; Oliveira, A.C.; Oliveira, M.M.; Oliveira, A.; Oliveira, W.; et al. Imunogenicidade e estruturas de um antígeno spike MERS-CoV de pré-fusão racionalmente projetado. Proc., 2017, 114, E7348–E7357. [Google Acadêmico] [Referência Cruzada]
- Watanabe, A.; Oliveira, L.; Pereira, E.R.; Oliveira, A.; Oliveira, M.; Pereira, J.D.; Oliveira, A.; Oliveira, D.; Oliveira, F.; Oliveira, A.; et al. Glicoproteína spike SARS-CoV-2 nativa-like expressa pela vacina ChAdOx1 NCoV-19/AZD1222. ACS Cent. 2021, 7, 594-602. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, L.; Oliveira, A.; Oliveira, A.; Oliveira, J.; Ribeiro, M.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Ribeiro, Z.; et al. Desenvolvimento de uma candidata vacinal inativada para SARS-CoV-2. Ciência 2020, 369, 77–81. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, M.; Ribeiro, M.; Oliveira, A.; Oliveira, C.; Ribeiro, P.; Oliveira, J.-G.; Oliveira, J.; Ribeiro, A.; Oliveira, A.; Oliveira, A.; A proteína spike de pré-fusão do SARS-CoV-2 estabilizada por seis em vez de duas prolinas é mais potente para induzir anticorpos que neutralizam variantes virais de preocupação. Proc., 2022, 119, e2110105119. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, F.; Ribeiro, A.; Oliveira, R.; Oliveira, M.; Tosse, L.; Oliveira, A.; Krammer, F. A introdução de duas prolinas e a remoção do local de clivagem polibásico conduzem a uma eficácia mais alta de uma vacina SARS-CoV-2 baseada em spike recombinante no modelo do rato. mBio 2021, 12, e02648-20. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Oliveira, P.A.; Oliveira, P.-L.; Désilets, A.; Oliveira, R.; Marsault, É. Inibidores de Serinoproteases Transmembrana Tipo II no Tratamento de Doenças do Trato Respiratório — Uma Revisão da Literatura de Patentes. Especialista. Opin. Tapinha. 2020, 30, 807-824. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, Z.; Oliveira, M.; Oliveira, G.; Oliveira, L.; Khan, H. Triagem virtual de produtos naturais contra a protease de serina transmembrana tipo II (TMPRSS2), o agente de priming do coronavirus 2 (SARS-CoV-2). Moléculas 2020, 25, 2271. [Google Acadêmico] [Referência Cruzada]
- Oliveira, P.N.; Oliveira, A.M.; Oliveira, V.; Akhrymuk, I.V.; Oliveira, J.; Oliveira, A.; Henrique, A.M.; Oliveira, J.L.; Oliveira, J.A.; Oliveira, F.; et al. A alfa 1 antitripsina é um inibidor da protease TMPRSS2 do SARS-CoV-2. Pathog. Imunizante. 2021, 6, 55-74. [Google Acadêmico] [Referência Cruzada]
- Oliveira, V.D.; Mattson, M.P. Jejum: Mecanismos Moleculares e Aplicações Clínicas. Metab celular. 2014, 19, 181–192. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, M.; Mordomo, A.E.; Oliveira, E.G.; Sahebkar, A.; O Efeito do Jejum ou da Restrição Calórica na Indução da Autofagia: Uma Revisão da Literatura. Envelhecimento Res. Rev. 2018, 47, 183–197. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Longo, V.D. Quantidade e Fonte de Proteína, Dietas Imitadoras de Jejum e Longevidade. Adv. Nutr. 2019, 10, S340–S350. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, G.; Ribeiro, A.; Oliveira, N.; Ribeiro, R.; Oliveira, F.; Oliveira, O.; Isidoro, C. Privação de arginina de aminoácido único desencadeia resposta autofágica de pró-sobrevivência no carcinoma ovariano SKOV3. Biomed. 2014, 2014, 505041. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, D.B.; Oliveira, H.T.; Oliveira, J.B.; Oliveira, V.T.; Ribeiro, L.A.; Oliveira, J.A.; Anderson, J.L. Associação do jejum periódico com a severidade mais baixa dos resultados COVID-19 na era pré-vacinal SARS-CoV-2: uma coorte observacional do registro INSPIRE. BMJ Nutr. Prev. Saúde 2022, 5, 145–153. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, J.; Oliveira, R.; Oliveira, J.; Igarashi, K. Diminuição de poliaminas com o envelhecimento e sua ingestão de alimentos e bebidas. J. Bioquímica. 2006, 139, 81–90. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, C.; Oliveira, D.; Pereira, J.; Oliveira, A.; Oliveira, C.; Oliveira, A.; et al. A indução de autofagia pela espermidina promove longevidade. Célula Biol. 2009, 11, 1305–1314. [Google Acadêmico] [Referência Cruzada]
- Verões, C.M.; Valentine, R.J. A exposição aguda ao calor altera a sinalização da autofagia em miotubos C2C12. Frente. Fisiol. 2020, 10, 1521. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.J.; Pereira, J.; Oliveira, L.P.; Kenny, G.P. Autofagia e calor: um papel potencial para a terapia de calor para melhorar a função autofágica na saúde e na doença. J. Appl. Fisiol. 2021, 130, 1–9. [Google Acadêmico] [Referência Cruzada]
- D’Arcy, M.S. Uma revisão dos flavonoides biologicamente ativos como indutores de autofagia e apoptose em células neoplásicas e como agentes citoprotetores em células não neoplásicas. Célula Biol. 2022, 46, 1179-1195. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Ozpolat, B. Regulação da Autofagia por Compostos Polifenólicos como Potencial Estratégia Terapêutica para o Câncer. Morte Celular Dis. 2014, 5, e1509. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.-R.; Pereira, Y.-S.; Oliveira, J.-J.; Oliveira, A.; Carvalho, C.-F.; Compostos naturais de ervas que podem potencialmente executar como indutores de autofagia para a terapia do câncer. Int. J. Mol. 2017, 18, 1412. [Google Acadêmico] [Referência Cruzada]
- Oliveira, F.; Oliveira, A.A.; Ribeiro, G.; Oliveira, E.; Oliveira, L.; Ribeiro, A.; Ribeiro, M.; Oliveira, M.C.; Madeo, F.; Kroemer, G. O café induz autofagia in vivo. Ciclo Celular 2014, 13, 1987–1994. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Ribeiro, R.; Oliveira, C.; Oliveira, A.; Oliveira, G.; Oliveira, D.N.; Ribeiro, C.; O resveratrol mimético de restrição proteica é um indutor de autofagia mais forte do que a fome de aminoácidos em células cancerosas de ovário. Mol Carcinog. 2017, 56, 2681–2691. [Google Acadêmico] [Referência Cruzada]
- Oliveira, G.; Oliveira, Z.; Oliveira, J.; Oliveira, Z.; Oliveira, C.; Zhang, C.; Os Efeitos da Metformina na Autofagia. Biomed. Farmacotera. 2021, 137, 111286. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Oliveira, J.; Oliveira, Z.; Oliveira, A.; Oliveira, A.; Oliveira, J.; Oliveira, J.; Oliveira, L.; Oliveira, A.; Ribeiro, J.; O estresse de retículo endoplasmático induzido por exposição ao frio regula a autofagia através da via de sinalização SIRT2/FoxO1. J. Celular. Fisiol. 2022, 237, 3960-3970. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.W.; Oliveira, A.A.; Oliveira, J.; Oliveira, J.A.; Oliveira, A.; Oliveira, B.-H.; Pereira, J.A.; Yen, P.M. A exposição crônica ao frio induz autofagia para promover oxidação de ácidos graxos, turnover mitocondrial e termogênese no tecido adiposo marrom. iScience 2021, 24, 102434. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.-C.; Oliveira, A.; Oliveira, A.-A.; Oliveira, A.; Sol, X.-Q. O pré-condicionamento de oxigênio hiperbárico reduz a lesão de isquemia-reperfusão por estimular a autofagia no neurócito. Cérebro Res. 2010, 1323, 149–151. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, P.; Oliveira, A.; Oliveira, X.; Oliveira, C.; Pereira, A.; Oliveira, M.; Fu, Z. O ozônio induz autofagia ativando PPARγ/MTOR em condrócitos de ratos tratados com IL-1β. J. Orthop. 2022, 17, 351. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Rezaei, N. Interleucina-6 e COVID-19 grave: uma revisão sistemática e meta-análise. Eur. Citocina Netw. 2020, 31, 44-49. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, D.B.; Oliveira, J.G.; Pretório, E.; Um papel central para microcoágulos de fibrina amiloide em COVID/PASC longo: origens e implicações terapêuticas. Bioquímica. 2022, 479, 537-559. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, E.; Oliveira, M.; Ribeiro, C.; Bezuidenhout, J.A.; Oliveira, J.G.; Oliveira, J.; Kell, D.B. Patologia persistente da proteína da coagulação em sequelas longas COVID/pós-agudas de COVID-19 (PASC) é acompanhada por níveis aumentados de antiplasmina. Cardiovasc. Diabetol. 2021, 20, 172. [Google Acadêmico] [Referência Cruzada]
- Oliveira, E.; Ribeiro, C.; Oliveira, J.G.; Oliveira, J.M.; Oliveira, S.O.; Oliveira, R.A.; Oliveira, J.; Oliveira, J.A.; Kell, D.B. Prevalência de sintomas, comorbidades, microcoágulos de fibrina amiloide e patologia plaquetária em indivíduos com COVID longa / sequelas pós-agudas de COVID-19 (PASC). Cardiovasc. Diabetol. 2022, 21, 148. [Google Acadêmico] [Referência Cruzada]
- Pereira, J.C.; Hawley, H.B. Trombocitopenia e trombose associadas à vacina: endoteliopatia venosa levando à micromacrotrombose venosa combinada. Medicina 2021, 57, 1163. [Google Acadêmico] [CrossRef] [PubMed]
- Principal, A.G.; Oliveira, J.B.; Orlando, F.A. O impacto da inflamação inicial do episódio COVID-19 entre adultos na mortalidade dentro de 12 meses após a alta hospitalar. Frente. 2022, 9, 891375. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, F.; Oliveira, E.; Pereira, E.A.; Oliveira, A.; Oliveira, R.; Ribeiro, E.; Ribeiro, S.S.; Ribeiro, J.; Oliveira, O.; Tanboğa, İ.H. Significância de MPV, RDW e PDW com a gravidade e mortalidade de COVID-19 e efeitos do uso de ácido acetilsalicílico. Clin. Ele. 2021, 27 10760296211048808. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, V.; Oliveira, F.; Oliveira, F.; Oliveira, P.; Oliveira, A.; Ribeiro, M.; O ácido acetilsalicílico é uma escolha segura e potencialmente útil para pacientes adultos com COVID-19? Drogas 2020, 80, 1383-1396. [Google Acadêmico] [Referência Cruzada]
- Clissold, S.P. Aspirina e derivados relacionados do ácido salicílico. Drogas 1986, 32, 8–26. [Google Acadêmico] [CrossRef] [PubMed]
- Pereira, O.; Ribeiro, A.; Enge, I. Complicações tromboembólicas na angiografia coronariana: prevenção com ácido acetil-salicílico. Acta Radiol. Diagn. 1977, 18, 555–560. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Brox, J.H.; O tempo de coagulação do sangue total em tubos plásticos: a influência do exercício, prostaciclina e ácido acetilsalicílico. Res. 1983, 29, 425–435. [Google Acadêmico] [Referência Cruzada]
- Oliveira, M.; Oliveira, J.; Oliveira, A.; Ribeiro, A.; Oliveira, A.; Nishimuro, S. Purificação e caracterização de uma forte enzima fibrinolítica (nattokinase) no natto de queijo vegetal, um alimento fermentado de soja popular no Japão. Bioquímica. Biófis. Res. Commun. 1993, 197, 1340–1347. [Google Acadêmico] [Referência Cruzada]
- Oliveira, R.-L.; Oliveira, J.-T.; Oliveira, J.-H.; Oliveira, L.Y.-L.; Chen, R.P.-Y. Capacidade de degradação amiloide da nattokinase de Bacillus subtilis natto. J. Agric. 2009, 57, 503–508. [Google Acadêmico] [Referência Cruzada]
- Oliveira, M.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, J.; Oliveira, A.; Ribeiro, J.; Oliveira, H.; Ribeiro, A.; O extrato de natto, um alimento fermentado japonês de soja, inibe diretamente infecções virais, incluindo SARS-CoV-2 in vitro. Bioquímica. Biófis. Res. Commun. 2021, 570, 21–25. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Ribeiro, A.; Oliveira, J.; Oliveira, J.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, R.; Ribeiro, A.; Kitamura, M. Efeito degradativo da nattokinase na proteína spike do SARS-CoV-2. Moléculas 2022, 27, 5405. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Oliveira, A.; Oliveira, A.; Ribeiro, A.; Oliveira, M.; Oliveira, J.F.; Ribeiro, A.; Uma dose única de nattokinase oral potencializa o perfil de trombólise e anticoagulação. Rep. 2015, 5, 11601. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, P.; Oliveira, A.C.; Pereira, A.C.; Oliveira, P.D.; Ribeiro, R.A.; Pereira, J.A.; Pentapati, S.S.K.; Ribeiro, G.; Oliveira, R.P.; Oliveira, M.M.; et al. Papel da ivermectina na prevenção da infecção por SARS-CoV-2 entre profissionais de saúde na Índia: um estudo de caso-controle correspondente. PLoS ONE 2021, 16, e0247163. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.C.; Dehgani-Mobaraki, P.; Os mecanismos de ação da ivermectina contra SARS-CoV-2 – Uma revisão extensiva. J. Antibiot. 2022, 75, 60–71. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, L.; Ribeiro, J.D.; Oliveira, M.G.; Oliveira, D.A.; Wagstaff, K.M.; O medicamento aprovado pela FDA ivermectina inibe a replicação do SARS-CoV-2 in vitro. Antivir. 2020, 178, 104787. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Oliveira, A.A.; Oliveira, A.; Pereira, J.E.; Oliveira, A.; Oliveira, R.A.; Tham, T.C. Ivermectina para prevenção e tratamento da infecção por COVID-19: uma revisão sistemática, meta-análise, e análise sequencial do ensaio para informar as diretrizes clínicas. Am. J. Ther. 2021 e 28 de 434. [Google Acadêmico] [Referência Cruzada]
- Oliveira, P.; Oliveira, J.G.; Oliveira, J.; Oliveira, J.; Marik, P.E. Revisão das evidências emergentes que demonstram a eficácia da ivermectina na profilaxia e no tratamento da COVID-19. Am. J. Ther. 2021, 28, e299–e318. [Google Acadêmico] [Referência Cruzada]
- Oliveira, M.; Oliveira, C.; Oliveira, A.; Oliveira, M.; Pereira, F.; Oliveira, M.-I.; Oliveira, A.A.; Oliveira, J.; Oliveira, A.-L.; Skoetz, N. Corticosteroides inalatórios para o tratamento de COVID-19. Banco de Dados Cochrane Syst. Rev. 2022, 3, CD015125. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Oliveira, J.S.; Oliveira, E.M.; Oliveira, K.M.I.; Bota, P.C.; Arbous, S.M. Uso de corticosteroides em pacientes COVID-19: Uma revisão sistemática e meta-análise em desfechos clínicos. Cuidados 2020, 24, 696. [Google Acadêmico] [Referência Cruzada]
- Goel, A.; Goyal, N.; Ribeiro, R.; Kumar, R. Corticosteroides sistêmicos para o manejo de ‘Long-COVID’: Uma avaliação após 3 meses de tratamento. Monaldi Arco Peito Dis. 2022, 92. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.I.; Oliveira, J.A.; Oliveira, A.; Oliveira, J.; Ribeiro, P.; Villar Gómez de las Heras, K. Anti-histamínicos e azitromicina como um tratamento para COVID-19 na atenção primária à saúde – Um estudo observacional retrospectivo em pacientes idosos. Pulm. Farmacol. Ther. 2021, 67, 101989. [Google Acadêmico] [Referência Cruzada]
- Oliveira, M.D.; Oliveira, A.; Ribeiro, A.C.; Oliveira, A.; Oliveira, J.D.; Oliveira, A.M.; Oliveira, C.W.; Chakraborty, R. Anti-histamínicos para sequelas pós-agudas da infecção por SARS-CoV-2. J. Enfermeira Pract. 2022, 18, 335-338. [Google Acadêmico] [Referência Cruzada]
- Pereira, R.L.; Oliveira, M.H.; Oliveira, R.; Oliveira, A.P.; Oliveira, D.; Ribeiro, Y.-S.J.; Ferreira, A.; Oliveira, J.A.; Ostrov, D.A. Identificação de anti-histamínicos antivirais para reaproveitamento de COVID-19. Bioquímica. Biófis. Res. Commun. 2021, 538, 173-179. [Google Acadêmico] [Referência Cruzada]
- Tantry, EUA; Ribeiro, J.P.; Gurbel, P.A. Mais evidências para o uso de aspirina em COVID-19. Int. J. Cardiol. 2022, 346, 107–108. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Ribeiro, A.; Oliveira, A.; Oliveira, A.; Mondal, P. Naltrexona um candidato terapêutico potencial para COVID-19. J. Biomol. Struct. Dyn. 2022, 40, 963-970. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Vidal, L.; Oliveira, A.; Oliveira, J.; Oliveira, G.; Lambert, J.S. Segurança e eficácia de naltrexona de baixa dose em uma coorte longa de Covid; um Estudo Pré-Pós Intervencionista. Cérebro. Comporte-se. Saúde 2022, 24, 100485. [Google Acadêmico] [Referência Cruzada]
- Oliveira, E.; Ribeiro, G.; Karalis, V. Colchicina para o tratamento de pacientes COVID-19: eficácia, segurança, e regimes de dosagem informados modelo. Xenobiotica 2021, 51, 643-656. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Oliveira, C.-H.; Pereira, M.; Oliveira, A.; Oliveira, R.; Oliveira, J.; Oliveira, Y.-G.; Oliveira, A.; Oliveira, E.H.; Oliveira, R.; Uso de colchicina em pacientes com COVID-19: uma revisão sistemática e meta-análise. PLoS UM 2021, 16, e0261358. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.B.; Pereira, R.V.; Rafique, A.M. Colchicina para o tratamento de lesão miocárdica em pacientes com doença 2019 do coronavirus (COVID-19) – uma droga velha com vida nova? JAMA Netw. Aberto 2020, 3, e2013556. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.T.L.; Oliveira, T.S.J.; Ribeiro, A.; Oliveira, J.W.; Oliveira, S.S.; Oliveira, A.C.; Oliveira, P.; Oliveira, D.C.; Ribeiro, J.; Oliveira, M.A.; et al. Eficácia e Segurança de Baixas Doses de Colchicina em Pacientes com Doença Coronariana: Uma Revisão Sistemática e Meta-Análise de Ensaios Randomizados. Eur. Coração J. 2021, 42, 2765-2775. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, J.R.; Oliveira, C.T.; Oliveira, A.; Oliveira, R.A.; Pereira, A.; Oliveira, A.; Oliveira, M.; Oliveira, L.; Oliveira, A.; et al. Metformina e Covid-19: revisão focada de mecanismos e literatura atual sugerindo benefício. Frente. Endocrinol. 2021, 12, 587801. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, C.T.; Ribeiro, J.B.; Oliveira, D.M.; Oliveira, J.L.; Oliveira, A.A.; Pereira, J.; Oliveira, A.; Oliveira, A.; Pereira, J.D.; Oliveira, J.J.; Tratamento ambulatorial da COVID-19 com metformina, ivermectina e fluvoxamina e o desenvolvimento de Covid longa ao longo de 10 meses de acompanhamento. medRxiv 2022. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Oliveira, L.; Pereira, J.B.; Frães-Toral, E.; Oliveira, G.; Oliveira, C.; Oliveira, F.; Oliveira, E.; Oliveira, J.; Oliveira, A.; Vitamina D: Um papel também na COVID-19 longa? Nutrientes 2022, 14, 1625. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, M.S.; Oliveira, M.; Pereira, E.; Oliveira, A.; Oliveira, A.; Oliveira, D.; Oliveira, O.K.; Oliveira, A.; Oliveira, A.; Balcãs, İ.İ.; et al. A suplementação rápida e eficaz da vitamina D pode apresentar melhores resultados clínicos em pacientes COVID-19 (SARS-CoV-2) alterando os soros, INOS1, IL1B, IFNg, cathelicidin-LL37, e ICAM1. Nutrientes 2021, 13, 4047. [Google Acadêmico] [Referência Cruzada]
- Oliveira, C.; Kraft, K. Viabilidade da vitamina C no tratamento da fadiga pós-viral com foco no COVID longo, com base em uma revisão sistemática da vitamina C IV na fadiga. Nutrientes 2021, 13, 1154. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, C.; Kraft, K. Estresse oxidativo e hiper-inflamação como principais impulsionadores de COVID-19 grave e COVID longo: implicações para o benefício de alta dose de vitamina C intravenosa. Pharm. 2022, 13, 899198. [Google Acadêmico] [Referência Cruzada]
- Tosato, M.; Oliveira, R.; Oliveira, A.; Oliveira, F.; Oliveira, V.; Coelho-Júnior, J.H.; Ribeiro, A.; Ribeiro, C.; Oliveira, J.; Pereira, E.; et al. Efeitos da suplementação de L-arginina mais vitamina C no desempenho físico, função endotelial, e fadiga persistente em adultos com COVID longo: Um ensaio clínico randomizado controlado simples-cego. Nutrientes 2022, 14, 4984. [Google Acadêmico] [Referência Cruzada]
- Oliveira, R.; Ribeiro, V.; Oliveira, P.; Oliveira, A.; Oliveira, M.; Oliveira, A.; Oliveira, G.; Oliveira, M.; Oliveira, M.; Oliveira, G.; Combinando L-arginina com vitamina C melhora os sintomas de COVID longo: A pesquisa LINCOLN. Pharm. 2022, 183, 106360. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, F.; Oliveira, C.; Ribeiro, P.; Ribeiro, Z.; Oliveira, M.; Oliveira, M.; Meinitzer, A. Diminuição dramática da vitamina K2 subtipo Menaquinone-7 em pacientes COVID-19. Antioxidantes 2022, 11, 1235. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Oliveira, V.; Oliveira, A.S.; Ribeiro, P.; Mandal, A. Perturbação conformacional da proteína spike de SARS-CoV-2 usando N-acetilcisteína, uma tesoura molecular: uma estratégia provável para combater COVID-19. ChemRxiv 2021. [Google Acadêmico] [Referência Cruzada]
- Oliveira, Z.; Puyo, C.A. N-Acetilcisteína para combater COVID-19: Uma revisão de evidência. Clin. Gestão de Riscos. 2020, 16, 1047-1055. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, J.K.; Oliveira, S.W.H.; Kua, K.P. N-Acetilcisteína como terapia adjuvante para COVID-19 – Uma perspectiva sobre o estado atual da evidência. J. Inflamm. Res. 2021, 14, 2993-3013. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, P.; Dutta, S. N-acetilcisteína como um regulador potencial de interrupções reprodutivas masculinas induzidas por SARS-CoV-2. Oriente Médio Fértil. 2022, 27, 14. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, A.; Oliveira, A.; Oliveira, V.; Oliveira, A.S.; Ribeiro, R.; Oliveira, A.; Oliveira, P.; Ribeiro, A.; Oliveira, C.; Oliveira, A.; N-acetilcisteína: uma ferramenta para perturbar a conformação da proteína spike do SARS-CoV-2. ChemRxiv 2021. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.N. O papel da deficiência de glutationa e variáveis MSIDS em COVID-19 longo. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT05371288 (acesso em 30 de setembro de 2022).
- Oliveira, V.; Oliveira, A.; Oliveira, A.; Oliveira, C.; Pereira, M.; Oliveira, F.; Pereira, S.-S.; Venketaraman, V. Suplementação de glutationa como uma terapia adjuvante em COVID-19. Antioxidantes 2020, 9, 914. [Google Acadêmico] [CrossRef] [PubMed]
- Polonikov, A. Deficiência endógena de glutationa como a causa mais provável de manifestações graves e morte em pacientes COVID-19. ACS Infectar. 2020, 6, 1558-1562. [Google Acadêmico] [Referência Cruzada]
- Oliveira, F.; Oliveira, A.; Pescarmona, G.P. O papel da glutationa na proteção contra a resposta inflamatória grave desencadeada pela COVID-19. Antioxidantes 2020, 9, 624. [Google Acadêmico] [Referência Cruzada]
- Oliveira, D.P.; Oliveira, G.M.; Pandi-Perumal, S.R. Possível aplicação de melatonina em COVID longo. Biomoléculas 2022, 12, 1646. [Google Acadêmico] [Referência Cruzada]
- Pereira, A.-A.; Oliveira, H.-Z.; Ribeiro, C.-M.; Pereira, S.-P.; Oliveira, L.-C.; Oliveira, C.-C.; Eficácia da melatonina no tratamento de pacientes com COVID-19: uma revisão sistemática e meta-análise de ensaios clínicos randomizados. J. Med. 2022, 94, 2102-2107. [Google Acadêmico] [Referência Cruzada]
- Oliveira, G.; Oliveira, P.; Oliveira, A.; Di Pierro, F.; Um papel para a quercetina na doença do coronavirus 2019 (COVID-19). Fitoterápica. Res. 2021, 35, 1230-1236. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Oliveira, A.; Pereira, A.; Oliveira, D.; Oliveira, A.; Oliveira, G.; Pereira, P.; Oliveira, A.; Kumar, P. Estudos de encaixe molecular de apigenina, Kaempferol, e quercetina como alvo potencial contra a proteína do receptor spike de SARS COV. J. Exp. Biol. 2022, 10, 144-149. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Üçüncü Ergun, N.; Oliveira, S.; Oliveira, A.; Oliveira, E.M.; Oliveira, M.A.; Oliveira, A.A.; Oliveira, A.; Kocataş, A. Tratamento de pacientes COVID-19 com quercetina: um ensaio prospectivo, único centro, randomizado, controlado. Turco J. Biol. 2021, 45, 518-529. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, A.; Oliveira, A.; Oliveira, J.; Ribeiro, A.; Oliveira, A.; Oliveira, A.; Oliveira, M.; Liu, L. Compostos fitoterápicos chineses contra SARS-CoV-2: Puerarina e quercetina prejudicam a ligação da proteína S viral ao receptor ACE2. Computação. Struct. Biotecnol. J. 2020, 18, 3518-3527. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.E.; Thimmulappa, R.K. Efeitos antivirais, imunomoduladores e anticoagulantes da quercetina e seus derivados: papel potencial na prevenção e gestão de COVID-19. J. Pharm. 2022, 12, 29–34. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Oliveira, U.A.; Oliveira, M.; Pascual-Figal, D.A.; Oliveira, A.; Abaidullah, S. Co-suplementação oral de curcumina, quercetina, e vitamina D3 como uma terapia adjuvante para sintomas leves a moderados de COVID-19 – Resultados de um ensaio clínico randomizado controlado aberto-piloto. Frente. Pharm. 2022, 13, 898062. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.-Y.; Oliveira, S.-L.; Oliveira, J.-C.; Oliveira, C.-C.; Hsiang, C.-Y. Emodin bloqueia a proteína spike do coronavírus SARS e a interação da enzima conversora de angiotensina 2. Antivir. 2007, 74, 92–101. [Google Acadêmico] [Referência Cruzada]
- Maideen, N.M.P. Medicina Profética-Nigella Sativa (Sementes de Cominho Preto) – Erva potencial para COVID-19? J. Farmacopunct. 2020, 23, 62-70. [Google Acadêmico] [Referência Cruzada]
- Rahman, M.T. Benefícios potenciais da combinação de suplementos de Nigella Sativa e Zn para tratar COVID-19. J. Erva Med. 2020, 23, 100382. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Oliveira, M.; Oliveira, J.C.; Oliveira, L.; Oliveira, M.; Maiti, S. nigellidine (Nigella sativa, semente de cominho-preto) acoplando-se a SARS CoV-2 Nsp3 e proteínas inflamatórias do hospedeiro podem inibir a replicação/transcrição viral e sinal de morte FAS-TNF via bloqueio TNFR 2021/36. Nat. Prod. 5817, 5822, <>-<>. [Google Acadêmico] [Referência Cruzada]
- Oliveira, R.; Ribeiro, A.; Oliveira, A.H.; Pintus, G. Potencial terapêutico do resveratrol em doenças hemostáticas COVID-19-associadas. Moléculas 2021, 26, 856. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, Z.; Oliveira, A.; Oliveira, F.; Oliveira, J.; Carteira, C.; Oliveira, C.; Oliveira, O.; Ribeiro, A.; Herbein, G. Resveratrol inibe a replicação do coronavírus HcoV-229E e SARS-CoV-2 em Vitro. Vírus 2021, 13, 354. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.E.; Bachari, K. Efeitos terapêuticos potenciais do resveratrol contra SARS-CoV-2. Acta Virol. 2020, 64, 276-280. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, R.M.; Oliveira, M.M.; Rhoda, D.A. Ensaio de prova de conceito randomizado duplo-cego controlado por placebo de resveratrol para tratamento ambulatorial da doença leve do coronavirus (COVID-19). Rep. 2022, 12, 10978. [Google Acadêmico] [Referência Cruzada]
- Oliveira, F.; Oliveira, A.A.; Oliveira, A.; Oliveira, M.; Oliveira, A.; Oliveira, J.; Oliveira, M.; Sahebkar, A. Efeitos potenciais da curcumina no tratamento da infecção COVID-19. Fitoterápica. Res. 2020, 34, 2911-2920. [Google Acadêmico] [CrossRef] [PubMed]
- Pereira, R.; Oliveira, A.; Oliveira, A.; Nagaraj, A.V.; Oliveira, G.; Oliveira, J.C.; Oliveira, R.; Suravajhala, P. Estudos comparativos de encaixe sobre curcumina com proteínas COVID-19. Preprints 2020, 2020050439. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.B.; Oliveira, A.; Ribeiro, V.; Ribeiro, G.B.N.; Dandapat, J. Catequina e curcumina interagem com a proteína S de SARS-CoV2 e ACE2 da membrana celular humana: Insights de estudos computacionais. Rep. 2021, 11, 2043. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.A.C.; Oliveira, G.G.; Celes, M.R.N. Curcumina como um tratamento potencial para COVID-19. Frente. Farmacol. 2021, 12, 2085. [Google Acadêmico] [Referência Cruzada]
- Vahedian-Azimi, A.; Oliveira, M.; Ribeiro, F.; Convidado, P.C.; Oliveira, M.; Oliveira, A.; Oliveira, M.; Oliveira, A.; Sahebkar, A. Eficácia da curcumina nos resultados de pacientes hospitalizados COVID-19: Uma revisão sistemática de ensaios clínicos. Nutrientes 2022, 14, 256. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.C.; Oliveira, M.A.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Abdelmohsen, S.M. Os efeitos da curcumina como suplemento dietético para pacientes com COVID-19: Uma revisão sistemática de ensaios clínicos randomizados. Droga Discov. Ther. 2022, 16, 14–22. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, F.; Oliveira, A.; Maier, J.A.; A pandemia de COVID-19: há um papel para o magnésio? Hipóteses e Perspectivas. Magnes. Res. 2020, 33, 21-27. [Google Acadêmico] [Referência Cruzada]
- Tang, C.-F.; Ribeiro, A.; Oliveira, R.-Q.; Oliveira, X.-X.; Kong, L.-D. Possibilidade de suplementação de magnésio para tratamento de suporte em pacientes com COVID-19. Eur. J. Pharm. 2020, 886, 173546. [Google Acadêmico] [Referência Cruzada]
- Oliveira, F.; Mercado, M.; Rodrigues, M.; Oliveira, C.; Oliveira, G.; Oliveira, D.; Ferreira, A.; Simental-Mendía, E.L.; Ribeiro, A.; Gamboa-Gómez, C.I.; Relação magnésio/cálcio e mortalidade por COVID-19. Nutrientes 2022, 14, 1686. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Oliveira, L.; Oliveira, A.; Oliveira, A.; Oliveira, J.; Oliveira, W.; Liu, M. Populações em áreas de baixo magnésio foram associadas com maior risco de infecção na transmissão precoce de COVID-19: um estudo de coorte retrospectivo nacional nos Estados Unidos. Nutrientes 2022, 14, 909. [Google Acadêmico] [Referência Cruzada]
- Tabatabaeizadeh, S.-A. Suplementação de zinco e mortalidade por COVID-19: uma meta-análise. Eur. J. Med. 2022, 27, 70. [Google Acadêmico] [CrossRef] [PubMed]
- Pereira, A.; Ribeiro, R.; Ribeiro, M.; Oliveira, A.; Oliveira, M.; Dutta, A.K.; Oliveira, A.; Oliveira, J.; Oliveira, P.; Prasad, R. Zinco e COVID-19: Base dos ensaios clínicos atuais. Traço Biol. Elem. 2021, 199, 2882-2892. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.S.; Oliveira, A.; Oliveira, G.; Ribeiro, A.; Ribeiro, B.; Os mecanismos da ação do zinco como um potente agente antiviral: a implicação terapêutica clínica em COVID-19. Antioxidantes 2022, 11, 1862. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, L.F.C.; Barros, A.N.A.B.; Leite-Lais, L. Risco nutricional da deficiência de vitamina D, vitamina C, zinco e selênio no risco e nos resultados clínicos de COVID-19: uma revisão narrativa. Clin. Nutr. ESPEN 2022, 47, 9–27. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, E.; Oliveira, F.; Oliveira, A.; Ribeiro, J.J.; Vinceti, M. Suplementação de zinco e selênio na prevenção e tratamento de COVID-19: Uma revisão sistemática dos estudos experimentais. J. Trace Elem. 2022, 71, 126956. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Oliveira, R.; Oliveira, D.; Oliveira, R.; Oliveira, A.; Oliveira, Z.; Ribeiro, A.; Oliveira, J.; Oliveira, F.W.; et al. Associações do uso habitual do óleo de peixe com o risco da infecção SARS-CoV-2 e resultados COVID-19-related no Reino Unido: estudo de coorte nacional baseado na população. medRxiv 2022. [Google Acadêmico] [Referência Cruzada]
- Pereira, J.R.; Ribeiro, V.; Jami, M.M. Óleo de peixe e tromboses COVID-19. J. Vasc. Linfata Venosa. Desord. 2020, 8, 1120. [Google Acadêmico] [Referência Cruzada]
- Oliveira, R.S.; Ribeiro, A.C.; Oliveira, A.G.; Waitzberg, D.L. Óleo de peixe parenteral: uma farmacoterapia adjuvante para a doença do coronavírus 2019? Nutrição 2021, 81, 110900. [Google Acadêmico] [Referência Cruzada]
- Oliveira, C.A.; Oliveira, C.; Oliveira, J.; Polite, A. Névoa cerebral associada à síndrome de COVID longa e quimiofog: luteolina para o resgate. Biofatores 2021, 47, 232–241. [Google Acadêmico] [Referência Cruzada]
- Oliveira, D.M.; Oliveira, G.; Pereira, J.L.; Oliveira, A.; Oliveira, J.-M.; Oliveira, A.; Nyandoro, S.S. Luteolin: Um bloqueador da entrada da pilha SARS-CoV-2 baseado no esquema complexo relaxado, simulação da dinâmica molecular, e metadynamics. Modelo J. Mol 2021, 27, 221. [Google Acadêmico] [CrossRef] [PubMed]
- Theoharides, T.C. COVID-19, mastócitos pulmonares, tempestades de citocinas, e ações benéficas da luteolina. Biofatores 2020, 46, 306–308. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Oliveira, L.; Oliveira, A.A.; Ribeiro, E.; Oliveira, P.; Oliveira, C.; Oliveira, G.; Oliveira, G.; Oliveira, F.; Oliveira, G.; Suplemento ultramicronizado de palmitoiletanolamina e luteolina combinado com treinamento olfativo para tratar o comprometimento olfativo pós-COVID-19: um ensaio clínico randomizado controlado por placebo multicêntrico duplo-cego. Curr. Neurofarmacol. 2022, 20, 2001-2012. [Google Acadêmico] [Referência Cruzada]
- Oliveira, P.; Oliveira, M.; Oliveira, P.; Menegazzi, M.; Hypericum perforatum (SJW) pode prevenir tempestade de citocinas em pacientes com COVID-19? Fitoterápica. Res. 2020, 34, 1471-1473. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, F.F.; Oliveira, D.; Oliveira, M.; Oliveira, A.; Ribeiro, N.; Oliveira, A.; Oliveira, G.; Oliveira, A.; Oliveira, J.; Ribeiro, E.R.; Hypericum Perforatum e seus ingredientes Hipericina e Pseudo-hipericina demonstram uma atividade antiviral contra SARS-CoV-2. Farmacêutica 2022, 15, 530. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.P.; Pereira, J.A.; Pereira, J.G.; Oliveira, A.; Langhi Prata, L.G.P.; Oliveira, J.R.; Oliveira, J.E.; Oliveira, E.O.; Oliveira, A.G.; Oliveira, J.B.; et al. Fisetin para COVID-19 em instalações de enfermagem qualificadas: ensaios senolíticos na era COVID. J. Am. Geriatr. 2021, 69, 3023-3033. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.O.; Oliveira, O.M.; Oliveira, O.T.; Oliveira, B.D.; Oliveira, J.J.; Oladiji, A.T. Kolaviron (Kolaflavanone), Apigenina, Fisetin como potenciais inibidores do coronavírus: In Silico Investigatio. Res. Sq. 2020. [Google Acadêmico] [CrossRef]
- Ribeiro, P.; Ribeiro, J.S.; Ribeiro, A.; Oliveira, A.; Oliveira, R.; Oliveira, A.; Ray, S. Visando a proteína spike de SARS-CoV-2 de COVID-19 com fitoquímicos de ocorrência natural: um estudo in silico para o desenvolvimento de drogas. J. Biomol. Struct. Dyn. 2021, 39, 6306-6316. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, C.; Como os medicamentos antienvelhecimento podem impulsionar as vacinas COVID em pessoas mais velhas. Natureza 2020, 586, 352–354. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, D.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Thomas, J. Terapia de combinação potencial usando vinte fitoquímicos de vinte plantas para prevenir a infecção por SARS-CoV-2: uma abordagem in silico. Virusdisease 2021, 32, 108–116. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, J.; Contratações, C.; Oliveira, A.; Dunne, E. Mistura de aromaterapia de tomilho, laranja, botão de cravo, e incenso aumenta os níveis de energia em pacientes femininas pós-COVID-19: um ensaio clínico randomizado, duplo-cego, controlado por placebo. Complemento. Ther. Med. 2022, 67, 102823. [Google Acadêmico] [Referência Cruzada]
- Oliveira, M.; O potencial da Moringa Oleifera como reforço imunológico contra a COVID 19. Terra Ambiente. 2021, 807 022008. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, C.A.; Oliveira, J.; Ribeiro, R.; Oliveira, A.; Al Mahtab, M.; Uma revisão de plantas medicinais com atividade antiviral disponível em Bangladesh e insight mecanicista em seus metabólitos bioativos em SARS-CoV-2, HIV e HBV. Frente. Pharm. 2021, 12, 732891. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.A.; Lima, C.R.; Oliveira, A.; Oliveira, C.Q.; Oliveira, C.S.; Oliveira, L.; Temerozo, J.R.; Oliveira, M.E.N.; Oliveira, S.S.G.; Oliveira, A.; et al. Agathisflavone, um biflavonóide natural que inibe a replicação do SARS-CoV-2 visando suas proteases. J. Biol. 2022, 222, 1015-1026. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Oliveira, M.G.; Oliveira, A.A.; Oliveira, J.; Oliveira, A.G.; Vlietinck, A.J. Óleo de noz-moscada: identificação e quantificação de seus constituintes mais ativos como inibidores da agregação plaquetária. J. Etnofarmacol. 1990, 29, 179–188. [Google Acadêmico] [Referência Cruzada]
- Le-Trilling, V.T.K.; Oliveira, D.; Oliveira, C.; Oliveira, R.; Oliveira, J.K.; Oliveira, A.S.; Oliveira, D.; Oliveira, A.; Oliveira, A.; Oliveira, A.; et al. Identificação de chás de ervas e seus compostos provocando atividade antiviral contra SARS-CoV-2 in Vitro. BMC Biol. 2022, 20, 264. [Google Acadêmico] [Referência Cruzada]
- Le-Trilling, V.T.K.; Oliveira, D.; Oliveira, C.; Oliveira, R.; Oliveira, J.K.; Oliveira, D.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, J.; Universalmente disponível chás de ervas baseados em sálvia e Perilla Elicit potente atividade antiviral contra variantes SARS-CoV-2 de preocupação por HMOX-1 Upregulation em células humanas. bioRxiv 2022. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.D.; Ribeiro, A.A.; Ribeiro, O.; Oliveira, V.; Ribeiro, O.; Abdulahi, A. SARS-COV-2 Spike Glycoprotein como alvo inibitório para triagem Insilico de composto natural. Biointerface Res. Appl. 2021, 11, 14974-14985. [Google Acadêmico]
- Oliveira, A.; Ribeiro, V.S.; Ribeiro, P.; Oliveira, A.; Oliveira, A.; Grover, A. Inibição dupla de SARS-CoV-2 Spike e protease principal através de uma droga reaproveitada, Rutina. J. Biomol. Struct. Dyn. 2022, 40, 4987-4999. [Google Acadêmico] [Referência Cruzada]
- Oliveira, F.M.; Oliveira, A.; Pereira, A.; Oliveira, C.; Oliveira, A.M.; Goyal, A.N.; Oliveira, J.A.; Oliveira, S.; O limoneno pode ser um possível candidato para avaliação como agente ou adjuvante contra infecção, imunidade e inflamação na COVID-19? Heliyon 2021, 7, e05703. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, M.E.; Ribeiro, A.; Oliveira, A.S.; Fikry, E. Eficácia do óleo essencial de casca de robusta de Agathis contra a COVID-19: Composição química, abordagens in silico e in vitro. Plantas 2022, 11, 663. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.; Ribeiro, Z.; Oliveira, M.; Oliveira, J.; Daneshmehr, M.A. Uma visão para o potencial terapêutico de polissacarídeos sulfatados derivados de algas e ácidos graxos poli-insaturados: Foco no COVID-19. J. Biol. 2022, 209, 244-257. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Oliveira, R.; Fatma, T. Explorando algas e cianobactérias como uma fonte natural promissora de droga antiviral contra SARS-CoV-2. Biomédica J. 2021, 44, 54-62. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, O.; Oliveira, A.; Oliveira, A.; Avni, D. Espirulina fotossinteticamente controlada, mas não espirulina solar, inibe a secreção de TNF-α: implicações potenciais para a terapia da tempestade de citocinas COVID-19-related. Biotechnol. 2021, 23, 149-155. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Pereira, R.P.; Oliveira, A.; Oliveira, P.; Pereira, J.A.; Kaushalendra; Pereira, J.C.; Ribeiro, J.R.; Pereira, M.A.; Oliveira, M.S.; Os metabólitos de algas podem ser um reforço imunológico contra a pandemia de COVID-19. Antioxidantes 2022, 11, 452. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, H.T.T.; Oliveira, M.; Oliveira, N.P.K.; Pereira, C.; Oliveira, E.; Efeito in vitro do extrato aquoso da folha de Taraxacum officinale na interação entre o receptor de superfície celular ACE2 e a proteína spike D2 do SARS-CoV-614 e quatro mutantes. Farmacêutica 2021, 14, 1055. [Google Acadêmico] [Referência Cruzada]
- Oliveira, V.P.; Oliveira, A.M.; Oliveira, A.A.; Oliveira, O.L.; Oliveira, A.A.; Ribeiro, A.B.; Oliveira, A.V.; Oliveira, A.A.; Oliveira, E.N.; Dobryak, T.A. Uma das possibilidades de otimizar a terapia de uma infecção pelo novo coronavírus em crianças com a inclusão de um extrato de raiz de marshmallow, flores de camomila, capim cavalinha, folhas de nogueira, capim-yarrow, casca de carvalho e capim-dente-de-leão: estudo de coorte prospectivo aberto comparativo. Pediatr. Cons. Med. 2022, 4, 322-330. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Oliveira, M.; Oliveira, A.L.; Oliveira, J.W.; Pereira, A.; Fröhlich-Nowoisky, J. Canela de Ceilão e seu principal composto Cinnamaldeído pode limitar a sinalização inflamatória e angiogênese em Vitro: implicações para o tratamento COVID-19. bioRxiv 2021. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Fröhlich-Nowoisky, J.; Oliveira, A.; Ackermann, M. Canela e extratos de lúpulo como imunomoduladores potenciais para casos graves de COVID-19. Frente. Planta Sci. 2021, 12, 589783. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Oliveira, D.; Oliveira, G.; Oliveira, A.; Convidado, P.C.; Oliveira, M.; Sahebkar, A. Canela: Um produto natural promissor contra COVID-19. Adv. Exp. Med. 2021, 1327, 191-195. [Google Acadêmico] [Referência Cruzada]
- Oliveira, M.; Taghipour, Z.; Oliveira, M.; Oliveira, M.; Oliveira, M.; Sadrai, S. Canela e seu possível impacto na COVID-19: o ponto de vista da medicina tradicional e convencional. Biomed. 2021, 143, 112221. [Google Acadêmico] [Referência Cruzada]
- Oliveira, V.; Oliveira, A.; Oliveira, A.; Oliveira, J.; Pereira, A.; Oliveira, M.; Oliveira, M.; Niazkar, R.H.; Os impactos favoráveis dos polifenóis da silibinina como terapia adjuvante na redução das complicações da COVID-19: uma revisão das evidências da pesquisa e dos mecanismos subjacentes. Biomed. Farmacotera. 2022, 154, 113593. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Ribeiro, C.; Oliveira, M.S.; Oliveira, F.; Oliveira, A.; Giofrè, S.V. Silibinina como ferramenta potencial contra SARS-Cov-2: In Silico Spike Receptor-Binding Domain e principal análise de acoplamento molecular de protease, e in vitro endothelial protective effects. Fitoterápica. Res. 2021, 35, 4616-4625. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Araújo, A.; Oliveira, A.; Ribeiro, P.; Uma revisão abrangente de Andrographis paniculata (Burm. F.) Nees e seus constituintes como compostos de chumbo potenciais para a descoberta da droga COVID-19. Moléculas 2022, 27, 4479. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Oliveira, A.; Pereira, A.; Oliveira, P.; Oliveira, P.; Oliveira, A.; Oliveira, A.; Oliveira, P.; Ribeiro, A.; Oliveira, J.; Atividade anti-SARS-CoV-2 do extrato de Andrographis paniculata e seu componente principal andrographolide em células epiteliais pulmonares humanas e avaliação da citotoxicidade em representantes de células de órgãos principais. J. Nat. Prod. 2021, 84, 1261-1270. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.A.; Ribeiro, J.C.; Jeyakanthan, J. Investigação computacional em fitoquímicos de Andrographis paniculata para avaliar sua potência contra SARS-CoV-2 em comparação com compostos antivirais conhecidos em ensaios de drogas. J. Biomol. Struct. Dyn. 2021, 39, 4415-4426. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.; Piriyachananusorn, N.; Oliveira, A.; Oliveira, A.; Ribeiro, C.; Oliveira, P.; Na-Ek, N.; Kanchanasurakit, S. Uso de Andrographis paniculata (Burm.f.) Parede. Ex Nees e risco de pneumonia em pacientes hospitalizados com doença leve do coronavirus 2019: um estudo de coorte retrospectivo. Frente. 2022, 9, 947373. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, Z.; Oliveira, M.; Oliveira, J.M.; Oliveira, A.A.; Oliveira, M.; Oliveira, D.; Yao, X. Identificação e avaliação do efeito inibitório do extrato de Prunella vulgaris na entrada do vírus SARS-Coronavirus 2. PLoS ONE 2021, 16, e0251649. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.A.; Abdel-Wadood, Y.A. O potencial da glicirrizina e extrato de alcaçuz no combate à COVID-19 e condições associadas. Fitomed. Mais 2021, 1, 100043. [Google Acadêmico] [Referência Cruzada]
- Oliveira, L.; Oliveira, M.; Oliveira, M.; Ribeiro, L.; Oliveira, C.S.; Oliveira, E.; Oliveira, D.; Ribeiro, A.; Oliveira, C.; Oliveira, O.; A glicirrizina inibe eficazmente a replicação do SARS-CoV-2 inibindo a protease principal viral. Vírus 2021, 13, 609. [Google Acadêmico] [CrossRef] [PubMed]
- Diomede, L.; Oliveira, M.; Oliveira, A.; Pereira, O.; Oliveira, M.; Salmona, M.; A atividade antiviral do alcaçuz pode ajudar a combater a infecção por COVID-19? Biomoléculas 2021, 11, 855. [Google Acadêmico] [Referência Cruzada]
- Gomaa, A. Avaliação dos efeitos terapêuticos potenciais de alcaçuz e Boswellia Serrata Goma em pacientes egípcios com COVID-19 como uma medicina complementar. 2022. Disponível online: https://clinicaltrials.gov/ct2/show/NCT04487964 (acesso em 30 de setembro de 2022).
- Oliveira, L.A.; Oliveira, J.-Y.; Oliveira, Y.S.; Oliveira, A.P.; Ribeiro, A.; Oliveira, P.A.; Oliveira, C.C.; Oliveira, V.; Goh, B.H. Licorice: Uma erva potencial na superação de infecções por SARS-CoV-2. J. Evídio. Baseado. Integr. Med. 2021/26, 2515690X21996662. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, J.; Oliveira, A.; Oliveira, M.; Oliveira, A.; Ribeiro, Y.-O.; Oliveira, R.; Oliveira, A.; Oliveira, E.; Oliveira, A.; Triterpenóides naturais de alcaçuz inibem potentemente a infecção por SARS-CoV-2. J. Adv. Res. 2021, 36, 201-210. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, N.; Pereira, P.; Oliveira, A.; Mandlecha, A. Resposta anti-inflamatória do extrato de cardamomo e predição da janela terapêutica em pacientes COVID-19 avaliando marcadores inflamatórios usando RT-PCR. Inflammofarmacologia 2022, 30, 883–894. [Google Acadêmico] [Referência Cruzada]
- Oliveira, C.; Oliveira, V.; Roviello, G.N. Bases moleculares do potencial terapêutico do cravo-da-índia (Syzygium aromaticum L.) e pistas para sua utilidade anti-COVID-19. Moléculas 2021, 26, 1880. [Google Acadêmico] [Referência Cruzada]
- Oliveira, J.R.; Oliveira, M.; Oliveira, A.; Oliveira, M.; Oliveira, M.; Oliveira, J.R.; Pahan, K. Eugenol, um componente do manjericão sagrado (Tulsi) e cravo-da-especiaria comum, inibe a interação entre o spike S2 do SARS-CoV-1 e o ACE2 para induzir respostas terapêuticas. J. Pharm neuroimune. 2021, 16, 743-755. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, F.; Oliveira, A.; Oliveira, E.; Ribeiro, C.; Ribeiro, A.; Oliveira, M.C.; Oliveira, E.; Dinelli, G. Espermidina do Gérmen de Trigo e Eugenol de Cravo em Combinação Estimulam a Autofagia In Vitro Mostrando Potencial no Suporte ao Sistema Imunológico contra Infecções Virais. Moléculas 2022, 27, 3425. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.A.; Oliveira, A.A.; Gomaa, M.A. Glycyrrhizin e ácidos Boswellic, os nutracêuticos dourados: multitargeting para o tratamento de COVID-19 leve-moderado e prevenção do comprometimento cognitivo pós-COVID. Inflammofarmacologia 2022, 30, 1977-1992. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Ribeiro, D.; Oliveira, A.; Oliveira, M.; Oliveira, A.; Oliveira, Z.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Oliveira, A.; Suplemento de gengibre reduziu significativamente o tempo de internação hospitalar em indivíduos com COVID-19. Nutr. Metab. 2022, 19, 84. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, A.; Ribeiro, R.; Oliveira, M.; Gharibzahedi, S.M.T. Alho (Allium Sativum L.): Um alimento terapêutico único potencial rico em compostos organosulfurados e flavonoides para combater a COVID-19. Nutr. 2020, 19, 124. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, M.M.; Oliveira, O.; Os efeitos do Allium Sativum na imunidade no âmbito da infecção COVID-19. Hipóteses 2020, 144, 109934. [Google Acadêmico] [Referência Cruzada]
- Oliveira, B.T.P.; Meu, T.T.A.; Oliveira, N.T.T.; Oliveira, J.T.; Oliveira, T.T.; Thi Phuong Loan, H.; Ribeiro, N.T.; Oliveira, T.T.V.; Oliveira, P.T.; Oliveira, V.P.; et al. Investigação sobre a resistência de compostos SARS-CoV-2 em óleo essencial de alho. ACS Ômega 2020, 5, 8312–8320. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Pereira, P.; Oliveira, A.; Oliveira, A.; Oliveira, C.; Ribeiro, A.; Oliveira, J.; Oliveira, A.; Chen, Z. Efeito do óleo essencial de alho em 97 pacientes hospitalizados com COVID-19: uma experiência multicêntrica. Pak. J. Pharm. 2022, 35, 1077-1082. [Google Acadêmico]
- Ribeiro, D.; Oliveira, M.; Oliveira, A.; Oliveira, S.; Uma visão focada no tomilho: propriedades biológicas, químicas e terapêuticas de uma erva mediterrânea indígena. Nutrientes 2022, 14, 2104. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.A.; Nagarajan, S.K.; Ribeiro, V.; Oliveira, V.; Oliveira, P.P.; Madhavan, T. Avaliação computacional dos principais componentes de óleos essenciais de plantas como inibidores potentes da proteína spike do SARS-CoV-2. J. Mol. 2020, 1221 128823. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, W.; Oliveira, R.; Oliveira, R.; Dilokthornsakul, P. Efeitos potenciais da própolis e do mel na prevenção e no tratamento da COVID-19: Uma revisão sistemática de estudos in silico e clínicos. J. Integr. 2022, 20, 114–125. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.A.; Oliveira, M.A.D.; Oliveira, J.M.; De Jong, D. Própolis e seu potencial contra os mecanismos da infecção SARS-CoV-2 e a doença COVID-19: Título da corrida: Própolis contra a infecção SARS-CoV-2 e COVID-19. Biomed. 2020, 131, 110622. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.M.; Kunugi, H. Própolis, mel de abelha, e seus componentes protegem contra a doença do coronavirus 2019 (COVID-19): uma revisão de In Silico, In Vitro, e estudos clínicos. Moléculas 2021, 26, 1232. [Google Acadêmico] [CrossRef] [PubMed]
- Ribeiro, A.; Oliveira, A.A.; Oliveira, M.; Pereira, F.L.; Tasca, J.I.; Oliveira, J.B.; Sforcin, J.M. Própolis Antiviral e Atividade Imunomoduladora: Uma revisão e perspectivas para o tratamento COVID-19. J. Pharm. 2021, 73, 281-299. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.C.; Oliveira, A.C.; Almeida, A.-C.G.; Oliveira, M.C.M.; Oliveira, J.; Oliveira, F.L.A.; Scorza, F.A. Atividade antiviral do extrato de própolis verde brasileiro contra a infecção por SARS-CoV-2 (Síndrome Respiratória Aguda Grave – Coronavírus 2): relato de caso e revisão. Clin. São Paulo 2021, 76, e2357. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, D.; Oliveira, J.; Oliveira, V.; Ribeiro, M.; De volta ao básico: Própolis e COVID-19. Derme. Ther. 2020, 33, e13780. [Google Acadêmico] [Referência Cruzada]
- Ribeiro, A.T.; Ribeiro, A.; Oliveira, A.; Oliveira, J.; Oliveira, C.; Ribeiro, E.; Oliveira, J.; Oliveira, D.; Vahidy, F.S. Tendências Contemporâneas na Incidência Nacional de Hemorragia Intracerebral Primária. AVC 2022, 53, e70–e74. [Google Acadêmico] [Referência Cruzada]
- Oliveira, A.; Oliveira, A.; Oliveira, J.; Ribeiro, G.; Oliveira, A.; Oliveira, R.; Bollmann, A. Dados nacionais de mortalidade para a Alemanha antes e durante a pandemia: Há um excesso de mortalidade que excede as mortes atribuídas à COVID-19. J. Infectar. 2022, 84, 834-872. [Google Acadêmico] [Referência Cruzada]
- Governo do Canadá, Statistics Canada. Painel de Mortes Provisórias e Excesso de Mortalidade no Canadá. Disponível online: https://www150.statcan.gc.ca/n1/pub/71-607-x/71-607-x2021028-eng.htm (acesso em 1º de outubro de 2022).
- Ribeiro, P.; Oliveira, A.; Oliveira, J.; Fernandes, M.; Oliveira, I.M.; A Introdução da Vacina contra Difteria, Tétano e Coqueluche e a Mortalidade Infantil na Guiné-Bissau Rural: Um Estudo Observacional. Int. J. Epidemiol. 2004, 33, 374–380. [Google Acadêmico] [CrossRef] [PubMed]
- Oliveira, M.; Oliveira, F.; Ribeiro, D.; Oliveira, M.; Oliveira, C.; Ribeiro, M.; De Marinis, Y. Transcrição reversa intracelular da vacina de Pfizer BioNTech COVID-19 MRNA BNT162b2 in vitro na linhagem celular do fígado humano. Curr. Questões Mol. 2022, 44, 1115–1126. [Google Acadêmico] [CrossRef] [PubMed]
|
Isenção de responsabilidade/Nota do editor: As declarações, opiniões e dados contidos em todas as publicações são exclusivamente do(s) autor(es) e colaborador(es) individualmente e não do MDPI e/ou do(s) editor(es). A MDPI e/ou o(s) editor(es) se isentam de responsabilidade por qualquer dano a pessoas ou propriedade resultante de quaisquer ideias, métodos, instruções ou produtos referidos no conteúdo.
|
