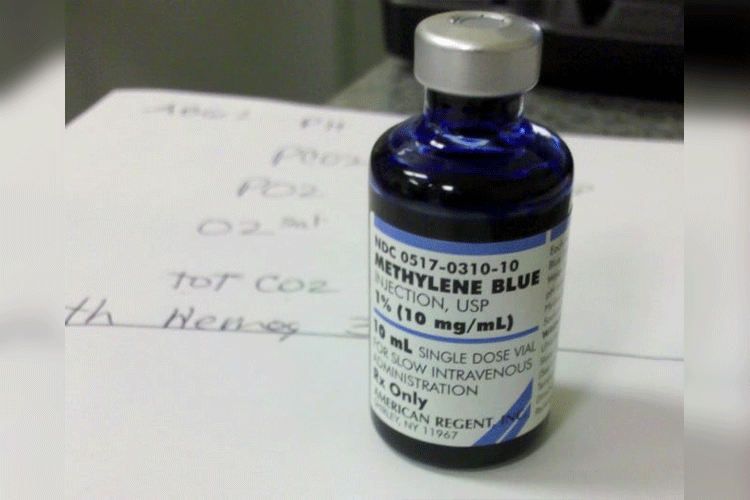
À medida que os casos de COVID Longa continuam a aumentar, é importante que a comunidade médica comece a se concentrar em estratégias terapêuticas de longo prazo que visam o ambiente inflamatório e isquêmico crônico observado nos cérebros dos infectados ou previamente infectados pelo COVID-19. Um dos agentes farmacológicos que a comunidade médica começa a observar para esse fim é o Azul de Metileno.
O que é Azul de Metileno?
O azul de metileno (MB) tem uma longa história de uso, embora nem sempre tenha sido utilizado para fins farmacêuticos. Foi sintetizado pela primeira vez em 1876 para uso como corante têxtil, mas já em 1891 foi investigado por suas aplicações medicinais. Uma de suas primeiras aplicações na área médica foi como cepa medicinal, mas logo se expandiu para ser usada em tratamentos.
Seus usos clássicos na área médica incluem tratamento para malária, envenenamento por monóxido de carbono e metemoglobinemia. No entanto, seu efeito sobre as mitocôndrias vem recebendo interesse crescente. Também há um interesse crescente na conexão entre a disfunção mitocondrial e os sintomas longos do COVID, aumentando o apelo do MB como potencial agente farmacológico e tratamento.
O Papel do Azul de Metileno no Tratamento da COVID Longa
MB desempenha um papel significativo na mitocôndria devido à sua capacidade de atuar como um ciclador redox catalítico. Este mecanismo permite que ele redirecione os elétrons na cadeia de transferência de elétrons mitocondrial do NADH para o citocromo c. Quando isso ocorre, a atividade do complexo IV é aumentada, o que promove a atividade mitocondrial enquanto atenua o estresse oxidativo.
Como o dano oxidativo, causado pela disfunção mitocondrial, prejudica o complexo IV, a capacidade do MB de aumentar a atividade do complexo IV desempenha um papel importante em sua capacidade de abordar e corrigir a disfunção mitocondrial.
O que são mitocôndrias?
Devido à capacidade do MB de influenciar as mitocôndrias e aumentar seu funcionamento, é importante considerar qual é o papel das mitocôndrias e por que sua disfunção desempenha um papel central nos sintomas longos do COVID.
As mitocôndrias são organelas que geram a maior parte do trifosfato de adenosina (ATP) usado pela célula. Praticamente cada grama de energia gerada em seu corpo vem do Ciclo de Krebs e da Cadeia de Transporte de Elétrons, ambos encontrados nas mitocôndrias.
Praticamente toda reação bioquímica requer a entrada de energia na forma de ATP. Sem ATP, bastam seis segundos para a célula começar a se deteriorar. A primeira coisa que se deteriora na célula sem ATP é a própria mitocôndria.
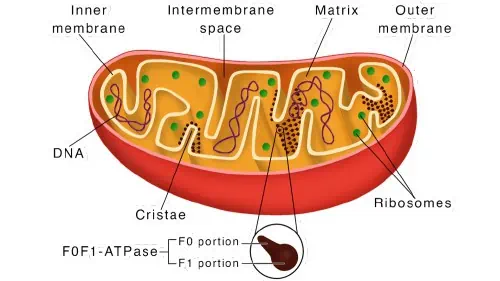
Alguns dos outros processos biológicos celulares nos quais as mitocôndrias desempenham papéis essenciais incluem apoptose, sinalização de cálcio, crescimento celular, geração de espécies reativas de oxigênio (ROS) e ciclo celular.
As mitocôndrias são muitas vezes apontadas como a “potência” da célula devido ao seu papel na produção de ATP, mas a verdade é que desempenham um papel muito mais importante no organismo, afetando sobretudo a imunidade.
As mitocôndrias detectam o ambiente celular e controlam a inflamação, o crescimento, a senescência e a morte. Com essas funções, as mitocôndrias equilibram as prioridades metabólicas entre crescimento, produção de energia, defesa e gerenciamento do estresse oxidativo. Existem muitas tarefas realizadas pelas mitocôndrias, e ter uma boa reserva mitocondrial garante que a célula permaneça flexível e multitarefa. A perda dessa flexibilidade pode contribuir para alterações relacionadas ao envelhecimento no sistema imunológico.
Além da Complexidade Insondável
A célula média no corpo humano tem entre 1000-2000 mitocôndrias, dependendo da energia metabólica que necessita para:
- Manter sua própria saúde.
- Fornecer para o resto do corpo o que foi projetado para fornecer.
Em contraste, as células cardiomiócitos têm 6-8000 mitocôndrias, e as células neurológicas são de longe as células metabolicamente mais ativas na fisiologia humana e contêm em média entre 2 a 3 milhões de mitocôndrias para:
- Manter sua própria saúde.
- Fornecer ao corpo uma rede neural funcional.
Dada a importância vital das mitocôndrias como geradoras de toda a sua energia “vital” bioquímica, sem mitocôndrias saudáveis, sua rede neural danificada não pode ser reparada.
Disfunção Mitocondrial
A disfunção mitocondrial ocorre quando há uma perda de função nas mitocôndrias e é uma observação comum em muitos distúrbios neurológicos que possuem lesões neurais crônicas e agudas. Algumas doenças que mostram disfunção mitocondrial incluem doenças neurodegenerativas e lesões cerebrais por falta de suprimento de sangue e oxigênio.
A disfunção mitocondrial desempenha um papel na indução de fatores que levam a distúrbios cerebrais, como inflamação, estresse oxidativo, alterações transcricionais e excitotoxicidade. Para distúrbios neurológicos, como lesão cerebral traumática, doença de Alzheimer, depressão, doença de Parkinson e acidente vascular cerebral, a disfunção mitocondrial contribui para a fisiopatologia da doença devido à diminuição da produção de energia e produção excessiva de espécies reativas de oxigênio (ROS). A produção excessiva de ROS leva ao estresse oxidativo, que é um fator importante que contribui para muitas doenças neurodegenerativas.
Estudos adicionais sobre o efeito da disfunção mitocondrial nesses distúrbios neurológicos descobriram que a restauração da função mitocondrial pode servir como um método de tratamento, com muitos estudos mostrando melhorias na função mitocondrial cerebral após o tratamento para a doença neurológica.
Efeitos a longo prazo do COVID-19 nas mitocôndrias do cérebro
Estudos descobriram que o COVID-19 pode afetar direta ou indiretamente o sistema nervoso central (SNC). Esses efeitos no SNC podem contribuir para os sintomas observados em pessoas com COVID-19, como alterações mentais e cognitivas graves de longo prazo, incluindo “névoa cerebral”.
Com a infecção, o genoma do RNA do SARS-CoV-2 se integra à matriz mitocondrial do hospedeiro, o que leva à replicação do vírus e ao aumento da carga viral. O RNA viral então sequestra a função mitocondrial para suprimir a resposta imune do corpo e promover ainda mais a replicação viral. À medida que a infecção continua, as células infectadas (que podem incluir neurônios) podem sofrer estresse oxidativo e influxo de íons de cálcio que podem levar à necrose, apoptose ou disfunção, juntamente com função mitocondrial prejudicada.
Os tecidos do cérebro requerem um suprimento imediato e constante de oxigênio para acompanhar seu metabolismo significativo. No entanto, o vírus SARS-CoV-2 pode causar hipóxia em algumas regiões do cérebro para beneficiar suas habilidades reprodutivas. Essa hipóxia pode então comprometer o metabolismo energético das células neuronais, levando à disfunção mitocondrial no tecido cerebral.
Esta teoria do efeito do vírus SARS-CoV-2 no SNC foi confirmada com autópsias que mostram a presença do coronavírus no SNC, especialmente no cérebro.
A Proteína Spike
O SARS-COV-2 infecta as células por meio de sua proteína spike, que se liga a um receptor de superfície na célula-alvo. Muitas pessoas infectadas desenvolverão anticorpos que neutralizam a proteína spike. No entanto, sabe-se que aqueles que produzem anticorpos que neutralizam uma cepa de COVID-19, mas não outra, têm chances aumentadas de aumento dependente de anticorpos (ADE) para a nova cepa, o que pode explicar os sintomas prolongados de COVID.
Há mais na proteína spike do que sua capacidade de permitir que o vírus se conecte a uma célula-alvo, com as próprias proteínas spike sendo tóxicas para a fisiologia humana. A proteína spike livre pode ter várias ações patológicas diretas nas células, incluindo a estimulação de mediadores pró-inflamatórios e vasoativos, especialmente fatores ativadores de plaquetas.
A proteína spike também pode danificar a barreira hematoencefálica (BHE) e alterar sua função induzindo a resposta inflamatória das células endoteliais microvasculares. Essas descobertas apoiam as observâncias de que o SARS-CoV-2 pode alterar o BBB e passar por ele para entrar no cérebro. O receptor de ligação à proteína spike SARS-CoV-2 (ACE2) também é amplamente expresso nas células endoteliais microvasculares do cérebro, e é por isso que geralmente atinge essas células, causando inflamação e sintomas neurológicos associados ao COVID-19.
A observação da proteína spike danificando e passando pela BHE não apenas apoia relatórios clínicos detalhando alterações neurológicas precoces, mas também serve como base para sintomas neurológicos de longo prazo.
Sintomas neurológicos comumente observados em pacientes com COVID-19
Aqueles com infecção por COVID-19 podem apresentar sintomas neurológicos como:
- Dor de cabeça;
- Náusea;
- Perda do paladar e do olfato;
- Breve perda de consciência;
- Confusão;
- AVC;
- Encefalite;
- Meningite;
- Convulsões.
Alguns desses sintomas são comuns em outras condições neurológicas, como doença de Alzheimer, esclerose múltipla e doença de Parkinson, fazendo com que aqueles com COVID prolongado sejam potencialmente diagnosticados erroneamente devido à imitação dos sintomas. Além disso, há uma preocupação crescente com os efeitos a longo prazo do SARS-CoV-2 no SNC e na função cognitiva. Especificamente, se o SARS-CoV-2 causar doenças neurodegenerativas ou se acelerar sua ocorrência prematuramente.
Proteína Spike de outras fontes
A pesquisa também mostra que a proteína spike pode ter esses mesmos efeitos de outras fontes da proteína spike, não apenas da própria infecção. Um estudo de 2021 descobriu que aqueles com COVID longa e que obtiveram a proteína spike de outra fonte mostraram proteína spike retida em monócitos.
Além disso, este estudo examinou pacientes que apresentaram sintomas de COVID longa após receberem a proteína spike e descobriram que eles responderam aos tratamentos destinados à COVID longa, apoiando a observância de que outras fontes da proteína spike podem causar COVID longa.
Estudos também mostram que a proteína spike de outras fontes conduz seletiva e potentemente a secreção de citocinas pró-inflamatórias em monócitos humanos. Isso apoia nossa crença de que a proteína spike está causando os problemas de inflamação e mitocôndria observados naqueles com COVID longa, e esta pesquisa explica por que estamos vendo pacientes com sintomas semelhantes, independentemente de terem obtido a proteína spike da infecção ou de outra fonte.
Azul de metileno como um tratamento de COVID longa
Uma quantidade significativa de evidências mostra que as alterações induzidas pelas mitocôndrias, como estresse oxidativo, transporte disfuncional de elétrons, desequilíbrio de Ca2+, tráfego mitocondrial prejudicado, mitofagia defeituosa e dinâmica mitocondrial alterada, mostram algum envolvimento em várias doenças cerebrais.
Como o MB é capaz de corrigir a disfunção mitocondrial, ele se mostra promissor como tratamento para a COVID Longa. Ele pode atingir e melhorar muitas áreas de dano mitocondrial, embora as duas áreas mais notáveis em relação ao tratamento de COVID longa incluam estresse oxidativo e neuroinflamação, porque têm maior impacto nos neurônios.
Os benefícios do MB em outras doenças neurológicas relacionadas à disfunção mitocondrial, como acidente vascular cerebral e doença de Parkinson, foram bem documentados. Também vimos melhorias em nossos pacientes ao tratar COVID longa com MB, apoiando ainda mais o uso de MB para corrigir casos de disfunção mitocondrial para aqueles com condições neurológicas.
Como o MB é administrado
O método ideal para administrar MB é por via intravenosa, pois permite uma maior concentração de fármaco disponível em comparação com a via oral.
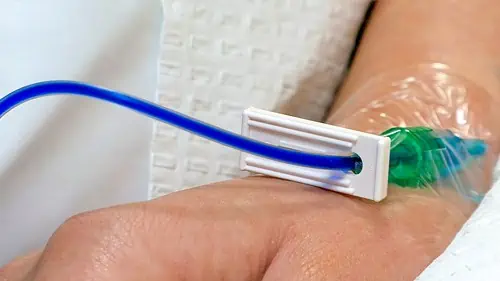
Uma vez administrado, o MB se acumula nos tecidos em concentrações significativas. Isso inclui o tecido cerebral, e a alta concentração permite que ele atravesse a BHE e potencialmente entre nas mitocôndrias neuronais. No entanto, o mecanismo pelo qual penetra nas mitocôndrias permanece obscuro.
Terapias baseadas em luz + azul de metileno
Em geral, a fotobiomodulação (PBM) e a terapia fotodinâmica (PDT) são dois métodos principais, que usam a luz na medicina e na odontologia.
- O PBM usa luz laser de baixo nível para induzir atividade celular saudável, incluindo proliferação e reparo.
- Em contraste, PDT usa luz laser de baixo nível combinada com um composto fotossensibilizador (PS) para causar a morte celular.
Devido a mecanismos semelhantes, mas não totalmente compreendidos, e à resposta bifásica da luz, resultados inesperados e complexos que ainda desafiam a explicação podem ser observados. Assim, ainda não foram desenvolvidos protocolos passo a passo que produzam resultados completos, confiáveis e reprodutíveis para a maioria das condições.
O que está claro, no entanto, é que a energia de baixo nível dos lasers e da luz LED usada é segura e fácil de usar.
Em relação ao COVID, ambas as modalidades devem ser teoricamente úteis, talvez até criticamente importantes se puderem ser combinadas.
Terapia Fotodinâmica (PDT)
Precisamos matar o vírus o mais rápido possível. Para isso, utiliza-se a Terapia Fotodinâmica com um Agente Fotossensibilizante que pode atingir e se concentrar no vírus, e um laser com uma frequência correspondente de energia (comprimento de onda) que é facilmente absorvido pelo Agente Fotossensibilizante.

O agente fotossensibilizador energizado agora liberará ROS que são mortais para o vírus. Idealmente, um protocolo adequadamente construído que aproveite essas propriedades eliminará rapidamente toda a carga viral do paciente e antes que o dano sistêmico seja criado.
Terapia Fotodinâmica (PDT) – O Básico
- Por razões que permanecem obscuras, certos compostos fotossensibilizantes possuem uma poderosa afinidade por células não saudáveis ou componentes específicos nelas, especialmente, mas não limitados à malignidade. Por exemplo: o azul de metileno é fortemente atraído pela malária.
- Uma vez administradas ao corpo, as células malignas/patogênicas visadas irão reter o composto fotossensibilizante, enquanto as células saudáveis são capazes de se livrar do composto fotossensibilizante durante um período de tempo especificado – “incubação”.
- O composto fotossensibilizador também deve conter os componentes moleculares necessários que, quando estimulados pela luz correta, são capazes de liberar as ERO necessárias, que matarão as células malignas ou patogênicas vizinhas.
Fotobiomodulação (PBM)
A fotobiomodulação (PBM) é outra abordagem terapêutica direcionada às mitocôndrias, mas seu mecanismo subjacente difere do MB. Devido a essas diferenças nos mecanismos, a combinação de PBM e MB pode oferecer melhores resultados do que qualquer uma das terapias individualmente.
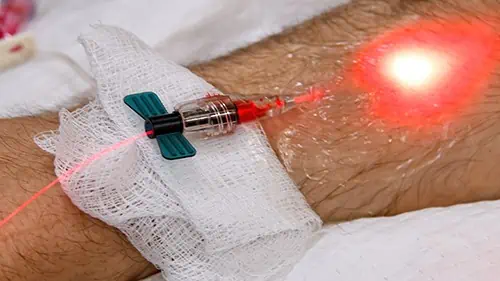
A PBM também é conhecida como terapia a laser de baixa intensidade e envolve a aplicação de laser de feixe vermelho (400-720 nm) ou infravermelho próximo (700-1000 nm) em tecidos biológicos. PBM pode modular vários processos biológicos devido à sua capacidade de atingir as mitocôndrias. O laser de baixa intensidade doa fótons ao complexo IV, o que aumenta sua atividade e, consequentemente, o consumo de oxigênio.
Fotobiomodulação (PBM) – O Básico
- Usando um comprimento de onda específico de luz que é absorvido por componentes específicos de células saudáveis, a atividade metabólica vital, a renovação celular saudável e equilibrada e as funções celulares internas podem ser estimuladas e aprimoradas. Em casos como COVID com ruptura mitocondrial grave, os fótons da luz correta estimularão a produção de ATP.
- Dado o dano celular onipresente causado pela interrupção da cadeia de transporte de elétrons da proteína de pico COVID nas mitocôndrias de células saudáveis e devido ao dano isquêmico do tecido causado pela inflamação sistêmica, estimular a atividade celular saudável, bem como a proliferação, pode melhorar e acelerar a recuperação de um paciente com COVID.
Considerações finais
A crescente pesquisa sobre o efeito da proteína spike SARS-CoV-2 na disfunção mitocondrial e, portanto, o papel das mitocôndrias nos sintomas de COVID longa, levou a uma necessidade crescente de tratamentos farmacológicos que reparam a função mitocondrial.
O azul de metileno é um agente farmacológico que apresenta resultados atraentes como tratamento para a COVID longa, que suspeitamos ser devido à sua capacidade de corrigir a disfunção mitocondrial. Quando combinado com a fotobiomodulação, outra abordagem terapêutica direcionada às mitocôndrias, o tratamento torna-se ainda mais eficaz.